Une réaction exothermique est une réaction qui dégage de l’énergie ce qui, par conséquent, augmente le degré énergétique du milieu environnant.
Lorsqu’une réaction chimique dégage de la chaleur dans un milieu, la température de ce milieu augmente. La température finale de la réaction est donc plus élevée que la température initiale.
On peut reconnaître une réaction exothermique de diverses façons:
On reconnaît une réaction exothermique lorsque, dans une équation chimique, la valeur énergétique associée (ou effet thermique) est intégrée du côté des produits de la réaction.
L'équation d'une réaction exothermique est de type:
|\text{Réactifs} \rightarrow \text{Produits}+ \text{énergie}|
La combustion du méthane est une réaction exothermique:
|CH_{4(g)} + 2 O_{2(g)} \rightarrow CO_{2(g)} + 2 H_{2}O_{(l)} + 810 kJ|
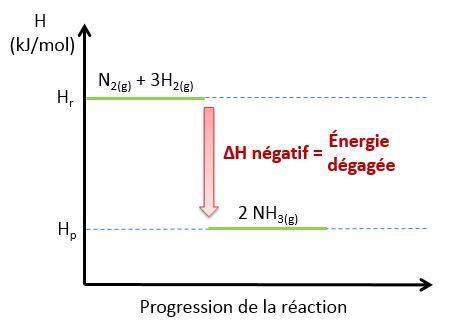
La synthèse de l'ammoniac est une réaction exothermique:
|N_{2(g)} + 3 H_{2(g)} \rightarrow 2 NH_{3(g)} + 95,4 kJ|
<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p>L’<a href="/fr/eleves/bv/chimie/l-enthalpie-et-la-variation-d-enthalpie-c1020">enthalpie</a> (H) d’une molécule se mesure en <strong>joules par mole (J/mol)</strong> ou en <strong>kilojoules par mole (kJ/mol)</strong>. Dans une réaction exothermique, l’enthalpie des réactifs est supérieure à celle des produits. Ainsi, la variation d'enthalpie (ΔH) est négative. </p>
</body></html>
Pour une réaction exothermique:
|H_{r} > H_{p}|
|\text{Réactifs} \rightarrow \text{Produits} \hspace {2 cm} \triangle H = \text {valeur négative}|
Voici deux exemples de réaction exothermique:
|CaO_{(s)} + CO_{2(g)} → CaCO_{3(s)} \hspace {2 cm} \triangle H = \text {- 178 kJ/mol}|
|N_{2(g)} + 3 H_{2(g)} → 2 NH_{3(g)} \hspace {2 cm} \triangle H = \text {-95,4 kJ/mol}|
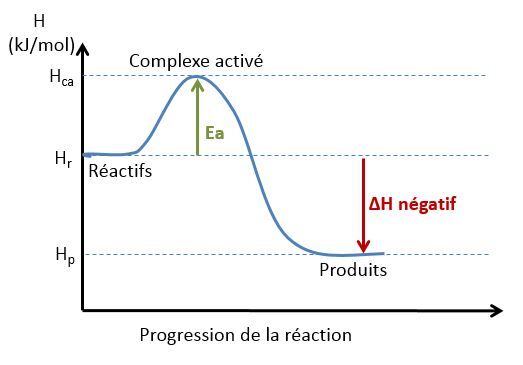
Voici un diagramme représentant une réaction exothermique et l’évolution de l’énergie lors de cette réaction :
<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p>Lors de la <strong>formation de liaisons </strong>dans une molécule, il y a toujours un <strong>dégagement d’énergie </strong>sous la forme de chaleur. Cette étape est toujours <strong>exothermique</strong>.</p>
<p>Il est possible d’affirmer qu’une réaction est <strong>exothermique </strong>lorsque l’<a href="/fr/eleves/bv/chimie/le-complexe-active-et-l-energie-d-activation-c1019"><strong>énergie d’activation</strong></a><strong> directe</strong> (|E_{ad}|) est <strong>plus faible</strong> que <strong>l’énergie d’activation inverse</strong> (|E_{ainv}|). On peut illustrer ces énergies par un <a href="/fr/eleves/bv/chimie/le-diagramme-energetique-c1018">diagramme énergétique</a>.</p>
</body></html>
Pour une réaction exothermique :
|E_{ad} < E_{ainv}|
<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p>Il existe plusieurs exemples de réactions exothermiques en chimie. Retenons principalement la majorité des <a href="/fr/eleves/bv/sciences/la-combustion-et-le-triangle-de-feu-s1065">combustions</a> lentes ou rapides et les <a href="/fr/eleves/bv/sciences/la-neutralisation-acidobasique-s1068">réactions de neutralisation</a>.</p>
</body></html>
Exemple de diagramme énergétique pour une réaction exothermique