La compressibilité est la propriété d'un gaz de pouvoir diminuer de volume sous l'effet d'une force.
L'expansion est la propriété d'un gaz de pouvoir se dilater pour occuper tout l'espace qui lui est disponible.
L'état gazeux est l'un des trois états dans lequel peut se trouver la matière, les autres étant les phases solide et liquide. À l'échelle macroscopique, un gaz est un ensemble d'atomes ou de molécules très faiblement liés et quasi-indépendants. Ainsi, dans l'état gazeux, la matière ne possède ni forme propre, ni volume propre. Un gaz tend plutôt à occuper tout le volume disponible.
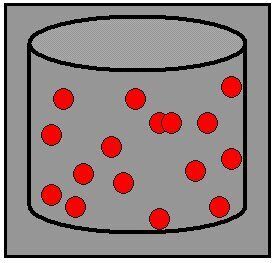
Ce modèle particulaire de l'état gazeux permet d'expliquer les propriétés de compressibilité et d'expansion des gaz.
La distance moyenne entre les particules d'un gaz est plus grande par comparaison avec la taille de ses particules. Cette distance peut être diminuée sous l'effet d'une force extérieure. On peut donc rapprocher les particules de gaz et ainsi en contenir une quantité équivalente dans un plus petit volume. Malgré ce rapprochement, les particules demeurent tout de même assez éloignées pour qu'elles continuent à conserver leur état gazeux. Cette propriété des gaz se nomme la compressibilité. On définit alors un gaz comme étant un fluide compressible. Les solides et les liquides ne possèdent pas cette propriété puisqu'ils ont un volume défini.
La compressibilité des gaz permet d'en entreposer de grandes quantités dans des espaces restreints. Par exemple, un plongeur peut respirer sous l'eau grâce à de l'air comprimé dans une bouteille. Un bouteille de plongée permet donc d'emporter sous l'eau environ 18 L d'air comprimé, ce qui est l'équivalent d'environ 3 600 L d'air à pression atmosphérique normale.
Lors du fonctionnement d'une pompe à vélo, l'air est comprimé avant d'être éjecté dans le pneu (à gauche). La compression de dioxyde de carbone dans la bouteille de champagne permet d'en faire sauter le bouchon lors de son ouverture (au centre). Un plongeur peut emporter une grande quantité d'air sous l'eau grâce à la compression de l'air dans sa bonbonne.
Étant donné que les particules de gaz sont très distancées, elles ont de l'espace pour se déplacer. Ainsi, elles se déplacent continuellement en ligne droite dans toutes les directions. Si le contenant où elles se trouvent n'a pas de volume fixe, l'impact des particules de gaz sur les parois du contenant crée une pression importante. Cela a pour conséquence d'augmenter le volume du contenant puisque les particules de gaz prendront tout l'espace qui leur est disponible. On dit alors qu'il se dilate. Plus un gaz se dilate, plus l'espace entre ses particules augmente. Ce phénomène d'expansion varie en fonction de la pression atmosphérique.
Un ballon-sonde est peu gonflé en basse altitude et il se gonfle en haute altitude en raison de la faible pression atmosphérique.



