Lorsqu'une substance basique est mise en solution aqueuse, la constante d'équilibre prend une forme particulière. Les scientifiques ont donc élaboré une variante de la constante d'équilibre à appliquer dans cette situation : la constante de basicité. Toutefois, une réaction à l'équilibre ne peut survenir qu'en cas de dissociation d'une base faible. En effet, les bases fortes se dissocient entièrement en solution ce qui constitue une réaction complète et donc irréversible.
La force d'un électrolyte, qu'il soit acide ou basique, correspond au pourcentage de dissociation de la substance en ions lorsque mise en solution.
Un électrolyte fort est un soluté qui se dissocie complètement dans l'eau.
Un électrolyte faible est un soluté qui ne se dissocie pas complètement dans l'eau.
<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p>Comme le stipulent les <a href="/fr/eleves/bv/chimie/les-theories-sur-les-acides-et-les-bases-arrheni-c1058">théories d'Arrhenius et de BrØnsted-Lowry</a>, les acides et les bases sont des substances qui libèrent des ions lorsqu'ils sont en solution aqueuse. Ce sont donc des <a href="/fr/eleves/bv/sciences/la-conductibilite-electrique-des-solutions-s1029">électrolytes</a>. Toutefois, ils ne subissent pas tous la dissociation électrolytique au même degré. C'est ce qui explique la présence d'électrolytes forts et d'électrolytes faibles. Avant d'étudier la constante de basicité, il est important de distinguer ces substances en fonction de leur force, puisque seuls les électrolytes faibles pourront être à l'état d'équilibre chimique.</p>
</body></html>
Un exemple d'électrolyte fort : l'hydroxyde de sodium |(\text{NaOH})|
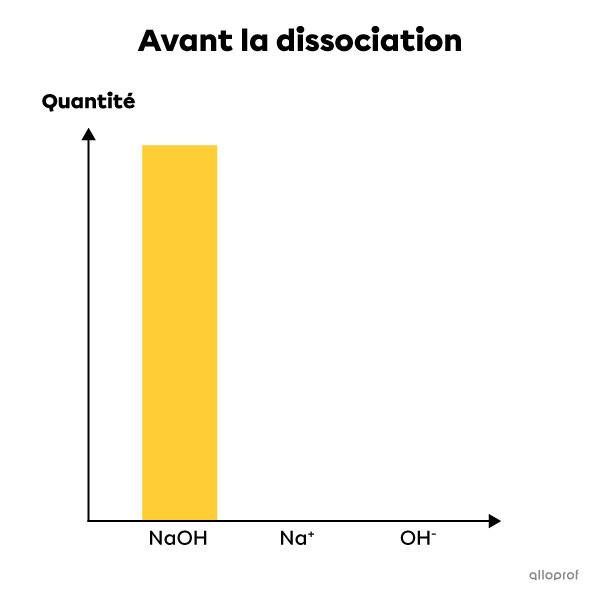
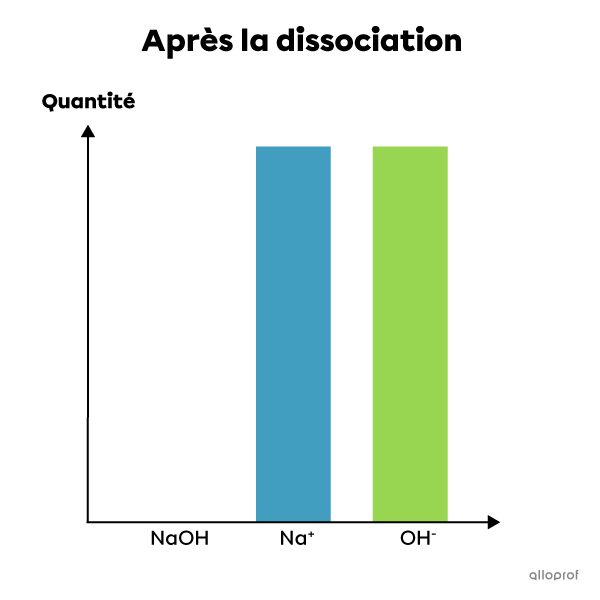
L'hydroxyde de sodium est un électrolyte fort. Lorsqu'il est mis en solution dans l'eau, il se dissocie complètement en ions. Ainsi, 100% de ses molécules se dissocient et forment des ions |\text{Na}^{+}| et |\text{OH}^{-}.| La solution contient alors le même pourcentage d'ions après la dissociation qu'il y avait de molécules de base avant la dissociation. Il s'agit donc d'une réaction complète qui ne peut être à l'équilibre. On écrit cette réaction chimique de la façon suivante :
|\text{NaOH}_{\text{(aq)}}^+ \rightarrow \text{Na}^+_{\text{(aq)}}+\text{OH}^-_{\text{(aq)}}|
Un exemple d'électrolyte faible : l'ammoniac |(\text{NH}_3)|
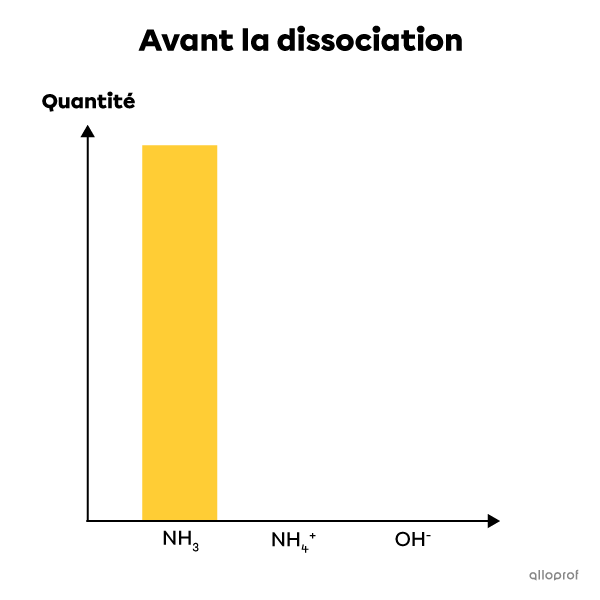
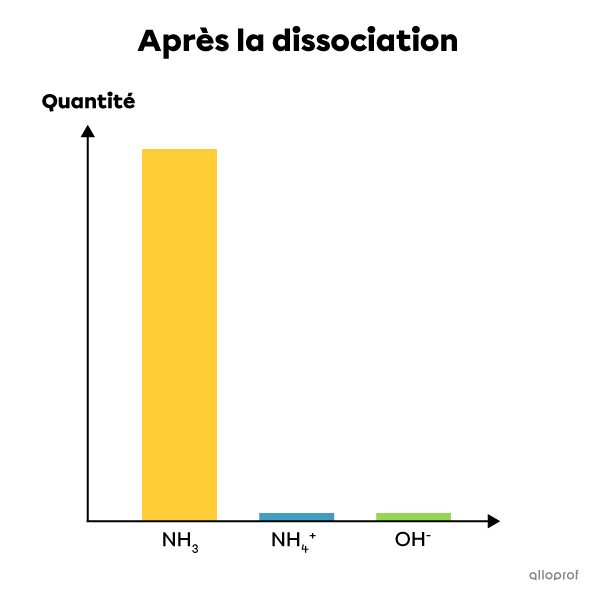
L'ammoniac est un électrolyte faible. Lorsqu'il est mis en solution dans l'eau, seule une partie de ses molécules se dissocie en ions. Ainsi, la plupart de ses molécules restent entières après la dissolution tandis qu'un très faible pourcentage de ses molécules se dissocient et forment des ions. La solution contient alors à la fois des réactifs (la molécule entière) et des produits (les ions en solution). Il s'agit donc d'une réaction incomplète et réversible qui est à l'équilibre. On écrit cette réaction chimique de la façon suivante :
|\text{NH}_{3(\text{aq})}+\text{H}_2\text{O}_{(\text{l})}\leftrightharpoons \text{NH}_{4{(\text{aq})}}^+ +\text{OH}^-_{(\text{aq})}|
Seuls les électrolytes faibles peuvent être à l'état d'équilibre.
On peut calculer le pourcentage de molécules qui se dissocient dans un électrolyte à l'aide de la formule du pourcentage d'ionisation:
|\text {Pourcentage d'ionisation} = \dfrac{[\text{OH}^{-}]}{[\text{B}]}\times 100|
où
|[\text{OH}^{-}]| : concentration des ions hydroxyde à l'équilibre |(\text {mol/L})|
|[\text{B}]| : concentration de la base avant la dissolution |(\text {mol/L})|
En plus de nous permettre de connaître le pourcentage d'ionisation de l'électrolyte, cette formule permet de déterminer la concentration des ions en situation d'équilibre. On peut alors calculer la constante de basicité.
La plupart des bases sont des bases faibles qui peuvent atteindre l'état d'équilibre en solution aqueuse. À l'équilibre, les molécules de la base se dissocient à la même vitesse que les ions formés se recombinent pour reformer les molécules de la base. On peut généraliser cette réaction de la façon suivante :
|\text{B}_{(\text{aq})} + \text{H}_{2}\text{O}_{(\text{l})} \rightleftharpoons \text{HB}^{+}_{(\text{aq})} + \text{OH}^{-}_{(\text{aq})}|
ou encore :
|\text{B}_{(\text{aq})} \rightleftharpoons \text{B}^{+}_{(\text{aq})} + \text{OH}^{-}_{(\text{aq})}|
La constante d'équilibre qui est associée à l'ionisation d'une base, nommée « constante de basicité », est alors exprimée de la façon suivante :
|K_{b}=\dfrac{[\text{B}^{+}][\text{OH}^{-}]}{[\text{B}]}|
où
|K_{b}| : constante de basicité
|[\text{B}^{+}]| : concentration de l'acide conjugué |(\text{mol/L})|
|[\text{OH}^{-}]| : concentration en ions hydroxyde dans l'eau |(\text{mol/L})|
|[\text{B}]| : concentration de la base non dissociée |(\text{mol/L})|
La constante de basicité |K_{b}| est une variante de la constante d'équilibre. La concentration de l'eau n'y apparait pas puisque l'eau est en phase liquide. La constante de basicité permet un classement des bases en fonction de leur force. En effet, plus la constante est grande, plus une base est forte.
1. Expression de la constante de basicité
On utilise l'équation théorique de la constante étant donné qu'on ne connait pas la base en solution.
|K_{b}=\displaystyle \frac{[B^{+}][OH^{-}]}{[B]}|
2. Calcul des concentrations des ions |OH^{-}|
|[H^{+}] = 10^{-pH}|
|[H^{+}] = 10^{-8,2}|
|[H^{+}] = 6,3\times 10^{-9} \text { mol/L}|
|K_{eau} = [H^{+}][OH^{-}]| donc
|[OH^{-}] = \displaystyle \frac{1\times 10^{-14}}{6,3\times 10^{-9}}|
|[OH^{-}] = 1,6\times 10^{-6} \text { mol/L}|
3. Tableau des concentrations à l'équilibre
| | |B| | |\rightarrow| | |B^+| | |+| | |OH^-| |
| [Initiale] | |\color{red}{0,20}| | |\huge \Rightarrow| | |\color{red}{0}| | |\huge +| | |\color{red}{0}| |
| [Variation] | |(-1,6\times 10^{-6})| | |(+1,6\times 10^{-6})| | |(+1,6\times 10^{-6})| | ||
| [Équilibre] | |0,19| | |1,6\times 10^{-6}| | |\color{red}{1,6\times 10^{-6}}| |
4. Calcul de la constante de basicité
|K_{b}=\displaystyle \frac{[1,6\times 10^{-6}][1,6\times 10^{-6}]}{[0,19]}|
|K_{b}=1,35\times 10^{-11}|
Les outils suivants peuvent être utiles dans les calculs de |K_{b}|: