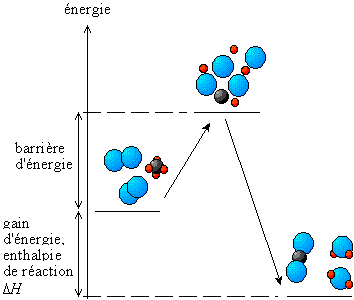
Le complexe activé est un état de transition instable et énergétique qui se forme lors de la transformation des réactifs en produits.
L'énergie d'activation est la quantité d'énergie minimale requise pour amorcer une réaction chimique, qu'elle soit endothermique ou exothermique.
<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p>Afin qu'une réaction chimique puisse se dérouler, les molécules de réactifs doivent entrer en collision. En effet, selon la <a href="/fr/eleves/bv/chimie/la-theorie-des-collisions-c1030">théorie des collisions</a>, certaines conditions sont nécessaires au déroulement d'une réaction. La collision des molécules de réactifs doit être efficace et non pas élastique, ce qui permet de former le complexe activé. Elle doit donc s'effectuer avec un minimum d'énergie, ce que l'on nomme l'énergie d'activation. Ces deux informations se retrouvent dans le tracé du <a href="/fr/eleves/bv/chimie/le-diagramme-energetique-c1018">diagramme énergétique</a> d'une réaction.</p>
</body></html>
Avant que les molécules de réactifs ne se transforment en produits, il se forme une molécule intermédiaire complexe très énergétique nommée complexe activé (Ca). Ainsi, au cours d'un très bref instant, les liaisons des réactifs s'affaiblissent tandis que de nouvelles liaisons commencent à se former. Cet état transitoire n'est que temporaire puisqu'il est fort instable. En effet, ce regroupement d'atomes intermédiaire n'est pratiquement pas détectable puisque les atomes ont tendance à rapidement reformer des molécules afin de retrouver la stabilité. De par son instabilité, le complexe activé possède toujours le maximum d'enthalpie d'une réaction. Il se retrouve donc toujours au sommet de la courbe d'un diagramme énergétique.
Le complexe activé se situe toujours entre les réactifs et les produits et au sommet de la courbe dans un diagramme énergétique.
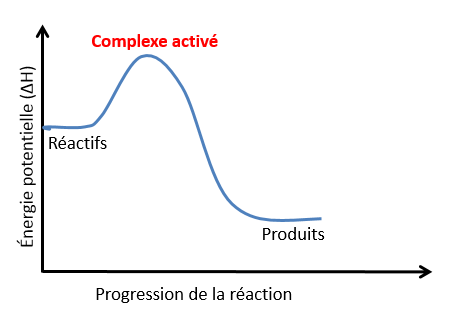
La formation du complexe activé résulte de la collision efficace de molécules de réactifs. Bien que certaines liaisons de réactifs soient encore présentes alors que certaines des produits se forment, on considère souvent cet état de transition comme étant le bref instant durant lequel toutes les liaisons chimiques ont disparues. On le symbolise donc par un amas d'atomes non liés qui se réorganiseront pour former de nouvelles molécules.
Le complexe activé est souvent représenté comme un groupe d'atomes non liés chimiquement. Dans le graphique ci-dessous illustrant la combustion du méthane, on peut constater que les liaisons chimiques des réactifs sont entièrement brisées avant que de nouvelles se forment dans les produits.
Pour que les réactifs puissent atteindre l'état de complexe activé, leurs collisions doivent se faire avec un minimum d'énergie qui correspond à l'énergie d'activation.
La formation du complexe activé implique le réarrangement des forces d'attraction entre les atomes des réactifs pour qu'ils se transforment en produits. Ce réarrangement nécessite une très grande quantité d'énergie. Ainsi, pour qu'une réaction chimique se produise, il faut que les réactifs reçoivent suffisamment d'énergie pour parvenir à former le complexe activé. Ce niveau d'énergie minimal nécessaire pour atteindre l'état de transition se nomme énergie d'activation et est symbolisé par Ea. Sa valeur correspond à la différence d'énergie entre le complexe activé et les réactifs.
La formule mathématique qui permet de calculer l'énergie d'activation d'une réaction directe est la suivante:
Ea=Hca−Hr
Soit le graphique ci-dessous:
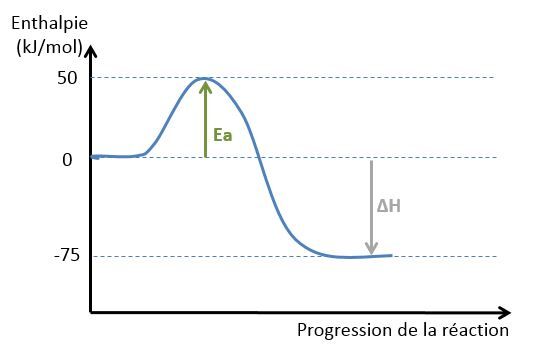
On peut calculer l'énergie d'activation de la façon suivante:
Ea=Hca−Hr
Ea=50−0
Ea=50kJ/mol
On peut aussi parler d’énergie d’activation inverse(Ea inv ). Il s’agit de la valeur qui correspond à la variation entre l’enthalpie des produits et celle du complexe activé. Cette énergie correspond à l’énergie d’activation dans la réaction inverse (les produits sont alors les réactifs et les réactifs deviennent les produits)
Pour calculer l'énergie d'activation d'une réaction inverse, on utilisera la formule mathématique suivante:
Eainv=Hca−Hp
Soit le graphique ci-dessous:
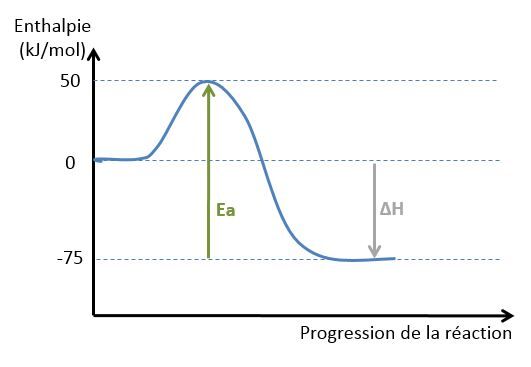
On peut calculer l'énergie d'activation de la réaction inverse de la façon suivante:
Eainv=Hca−Hp
Eainv=50−(−75)
Eainv=125kJ/mol
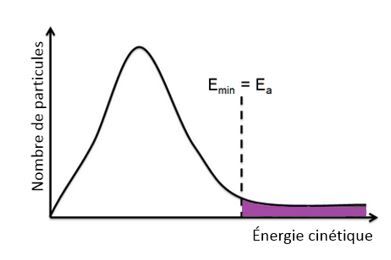
On peut aussi représenter l’énergie d’activation grâce au graphique illustrant le nombre de molécules en fonction de l’énergie cinétique. Dans ce cas, la barrière d'énergie correspond à l'énergie d'activation. Toutes les molécules possédant ce minimum d'énergie ou une quantité supérieure auront des collisions efficaces et pourront réagir.
Les molécules qui constituent les réactifs doivent donc posséder suffisamment d'énergie pour être capables de briser les forces ou les liens qui les unissent, et ce, dans le but de former de nouvelles liaisons et de former de nouvelles molécules. Cette énergie minimum correspond à l'énergie d'activation. La zone en mauve sur le graphique ci-dessous correspond à l'ensemble des molécules de réactifs qui ont une énergie suffisante pour pouvoir réagir.
La valeur de l'énergie d'activation peut nous aider à estimer la vitesse relative d'une réaction. En effet, une valeur d'énergie d'activation élevée indique une réaction lente. Dans le cas d’une réaction lente, peu de réactifs (l’aire sous la courbe à droite de l’énergie d’activation) ont une énergie cinétique suffisante pour franchir la barrière et former de nouveaux produits. Dans le cas inverse, une valeur d’énergie d'activation qui est faible indique une réaction rapide.
Le graphique de gauche illustre une réaction relativement lente puisque l'énergie d'activation y est élevée alors que celui de droite illustre une réaction rapide puisque l'énergie d'activation y est faible.

<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p>Certains facteurs peuvent influencer le niveau d'énergie minimale à atteindre pour l'amorce d'une réaction:<br>
<a href="/fr/eleves/bv/chimie/les-facteurs-qui-influencent-la-vitesse-de-reacti-c1028">Les facteurs qui influencent la vitesse de réaction</a></p>
</body></html>