Une réaction endothermique est une réaction qui absorbe de l’énergie provenant de l'environnement ce qui, par conséquent, abaisse le degré énergétique du milieu.
Lorsqu’une réaction chimique absorbe de la chaleur, la température du milieu environnant diminue. La température finale est alors moins élevée que la température initiale. C’est donc le milieu qui est responsable de ce transfert d’énergie.
On peut reconnaître une réaction endothermique de diverses façons:
On reconnaît une réaction endothermique lorsque, dans une équation chimique, la valeur énergétique associée (ou effet thermique) est intégrée du côté des réactifs de l’équation.
L'équation d'une réaction endothermique est de type:
|\text{Réactifs} + \text{énergie} \rightarrow \text{Produits}|
La fusion de l'eau est une réaction endothermique:
|H_{2}O_{(s)} + 6 kJ \rightarrow H_{2}O_{(l)}|
La décomposition de l'ammoniac est une réaction endothermique:
|2 NH_{3(g)} + 95,4 kJ \rightarrow N_{2(g)} + 3 H_{2(g)}|
<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p>L’<a href="/fr/eleves/bv/chimie/l-enthalpie-et-la-variation-d-enthalpie-c1020">enthalpie</a> (H) d’une molécule se mesure en <strong>joules par mole (J/mol) </strong>ou en <strong>kilojoules par mole (kJ/mol). </strong>Dans une réaction endothermique, l’énergie totale des réactifs, ou l’enthalpie (H) totale, est inférieure à celle des produits. Ainsi, la variation d'enthalpie (ΔH) est positive.</p>
</body></html>
Pour une réaction endothermique:
|H_{r} < H_{p}|
|\text{Réactifs} \rightarrow \text{Produits} \hspace {2 cm} \triangle H = \text {valeur positive}|
Voici deux exemples de réaction endothermique:
|CaCO_{3(s)} \rightarrow CaO_{(s)} + CO_{2(g)} \hspace {2 cm} \triangle H = \text {+ 178 kJ/mol}|
|2 NH_{3(g)} \rightarrow N_{2(g)} + 3 H_{2(g)} \hspace {2 cm} \triangle H = \text {+95,4 kJ/mol}|
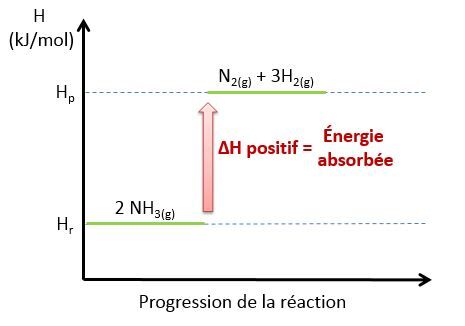
Voici un diagramme représentant la réaction endothermique de la décomposition de l’ammoniac et l’évolution de l’énergie lors de cette réaction.
<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p>Lors de la <strong>rupture de liaisons </strong>dans une molécule, il y a toujours une <strong>absorption d’énergie </strong>sous la forme de chaleur. Cette étape est toujours <strong>endothermique</strong>.</p>
<p>Il est possible d’affirmer qu’une réaction est <strong>endothermique </strong>lorsque <strong>l’<a href="/fr/eleves/bv/chimie/le-complexe-active-et-l-energie-d-activation-c1019">énergie d’activation</a></strong><strong> directe </strong>(|E_{ad}|) est <strong>plus élevée </strong>que <strong>l’énergie d’activation inverse</strong> (|E_{ainv}|). On peut illustrer ces énergies par un <a href="/fr/eleves/bv/chimie/le-diagramme-energetique-c1018">diagramme énergétique</a>.</p>
</body></html>
Pour une réaction endothermique:
|E_{ad} > E_{ainv}|
Il existe plusieurs exemples de réactions endothermiques, notamment la majorité des décompositions chimiques que ce soit par l’apport de la chaleur, de la lumière ou de l’électricité (électrolyse).
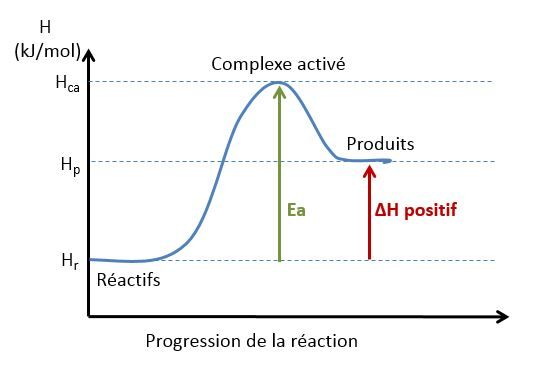
Exemple de diagramme énergétique pour une réaction endothermique