-
Un catalyseur est une substance qui augmente la vitesse d’une réaction chimique en diminuant son énergie d’activation sans être consumée dans le processus.
-
La catalyse est le processus d’augmentation de la vitesse de réaction à l’aide d’un catalyseur.
L’un des principes de la théorie des collisions veut que seules les particules dont l’énergie cinétique est égale ou supérieure à l’énergie d’activation puissent subir des collisions efficaces. Un catalyseur modifie le mécanisme réactionnel de manière à générer un plus grand nombre de collisions efficaces. Par conséquent, l’énergie d’activation nécessaire pour transformer les réactifs en produits diminue.
Le graphique suivant compare les diagrammes énergétiques d’une réaction chimique avec et sans catalyseur. L’énergie d’activation de la réaction catalysée |(E_{a_{cat}})| est nettement inférieure à l’énergie d’activation non catalysée |(E_a).| Lorsque l’énergie d’activation diminue, le nombre de collisions efficaces ainsi que la vitesse de réaction augmentent.
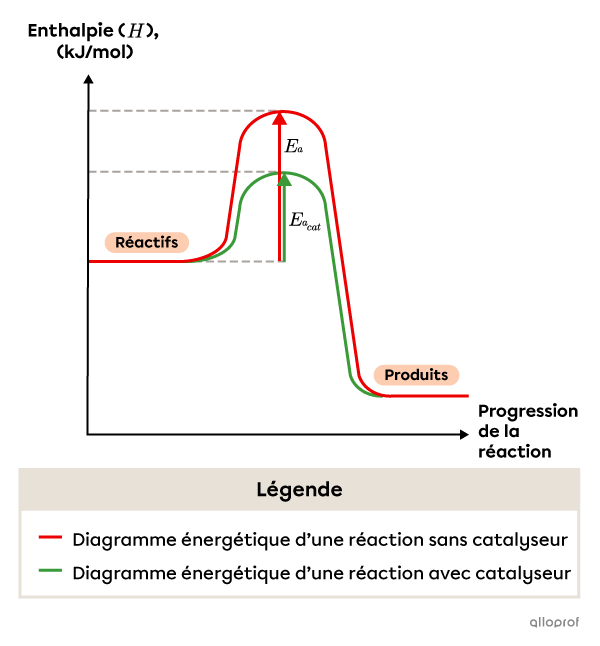
Par exemple, un mécanisme de réaction en deux étapes peut devenir un mécanisme de réaction en quatre étapes lorsqu’un catalyseur est ajouté. Globalement, le mécanisme de réaction catalysé a une énergie d’activation plus faible que le mécanisme de réaction non catalysé.
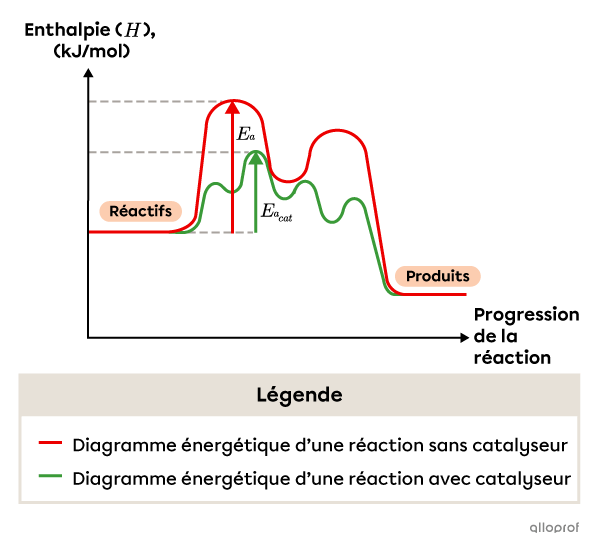
En raison de la diminution de l’énergie d’activation, le nombre de particules possédant suffisamment d’énergie cinétique pour faire des collisions efficaces augmente. Ceci est démontré par la courbe de distribution de Maxwell-Boltzman suivante.
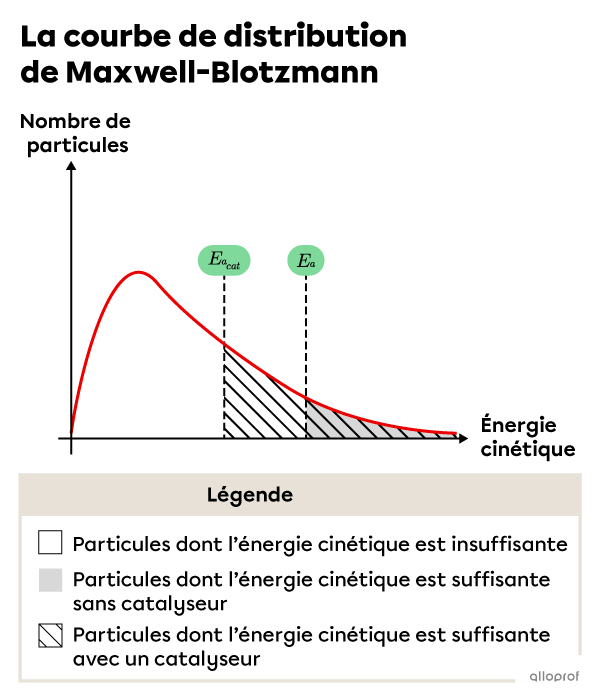
Les particules de la zone non ombrée ont une énergie cinétique inférieure à l’énergie d’activation requise. Les particules de la zone ombrée ont une énergie cinétique égale ou supérieure à l’énergie d’activation requise sans catalyseur. Les particules de la zone hachurée ont une énergie cinétique égale ou supérieure à l’énergie d’activation requise avec un catalyseur.
La liste suivante présente quelques principes importants à propos des catalyseurs.
- Les catalyseurs ne modifient pas l’équation globale de la réaction : la formule chimique des réactifs et des produits souhaités n’est pas affectée par l’utilisation d’un catalyseur.
Équation chimique globale sans catalyseur :
||\text{A} + \text{B} \rightarrow \text{C}||
Équation chimique globale avec un catalyseur :
||\text{A} + \text{B} + \cancel{\text{Catalyseur}} → C + \cancel{\text{Catalyseur}}\\\\ \Rightarrow \text{A} + \text{B} \rightarrow \text{C}||
Une autre façon fréquemment utilisée pour indiquer l’utilisation d’un catalyseur est d’écrire le mot catalyseur ou la formule chimique de la substance utilisée comme catalyseur au-dessus de la flèche dans l’équation chimique.
||A + B \xrightarrow{\text{Catalyseur}} C|| -
Les catalyseurs n’affectent pas la variation d’enthalpie de la réaction.
||\Delta H = \Delta H_{(cat)}|| -
Les catalyseurs modifient le mécanisme de réaction, ce qui entraine une modification de la constante de vitesse |(k)| ainsi que de la loi de vitesse.
-
Les catalyseurs réduisent l’énergie d’activation des réactions directes et inverses, ce qui signifie que les deux vitesses de réaction sont augmentées.
-
Les catalyseurs sont reformés et peuvent être récupérés à la fin de la réaction pour être réutilisés.
-
Les catalyseurs n’affectent pas la position de l’équilibre d’une réaction chimique, mais ils peuvent faire en sorte que l’équilibre soit atteint plus rapidement.
-
Les substances appelées inhibiteurs ont l’effet inverse des catalyseurs : elles diminuent la vitesse de réaction.
Les catalyseurs sont couramment utilisés dans de nombreuses industries pour accélérer des réactions chimiques de manière rentable et respectueuse de l’environnement. L’utilisation d’un catalyseur peut :
-
diminuer la quantité d’énergie nécessaire pour effectuer une réaction;
-
diminuer la quantité de déchets chimiques générés par la réaction, y compris les gaz à effet de serre et autres polluants;
-
augmenter le rendement d’une réaction en augmentant la quantité de réactifs transformés en produits souhaités, ce qui réduit la quantité initiale requise de réactifs.
Les procédés catalytiques sont utilisés dans la production de nombreuses substances chimiques et de matériaux synthétiques dans le secteur de l’énergie, dans la recherche pharmaceutique et médicale, dans la science alimentaire, etc.
L’Aspirine, ou l’acide acétylsalicylique |(\text{CH}_3\text{COOC}_6\text{H}_4\text{COOH}),| est synthétisée à partir de deux réactifs, soit l’acide salicylique |(\text{HOC}_6\text{H}_4\text{COOH})| et l’anhydride acétique |(\text{CH}_3\text{COOCOCH}_3).| L’acide sulfurique |(\text{H}_2\text{SO}_4)| est utilisé comme catalyseur.
||\text{HOC}_6\text{H}_4\text{COOH} + \text{CH}_3\text{COOCOCH}_{3} \xrightarrow{\text{H}_2\text{SO}_4} \text{CH}_3\text{COOC}_6\text{H}_4\text{COOH} + \text{CH}_3\text{COOH}||
Sans catalyseur, l’énergie d’activation de cette réaction est trop élevée et sa vitesse est très lente. De plus, une partie des réactifs est gaspillée en ne réagissant pas ou en réagissant pour former des produits non désirés.
Avec un catalyseur, la réaction utilise un mécanisme qui permet à une grande partie des réactifs d’être transformés en produits désirés. Grâce à la diminution de l’énergie d’activation, la réaction peut se produire plus rapidement et à une température plus basse.

Source : Ground Picture, Shutterstock
Les catalyseurs sont généralement classés en deux catégories : les catalyseurs hétérogènes et les catalyseurs homogènes. Les catalyseurs homogènes comprennent les catalyseurs biologiques, également appelés enzymes.
Un catalyseur hétérogène est un catalyseur utilisé dans un état différent de celui des réactifs.
Les catalyseurs hétérogènes sont généralement des métaux ou des composés à base de métaux. Ils sont généralement à l’état solide et utilisés pour catalyser des réactions où les réactifs sont à l’état liquide, aqueux ou gazeux. La catalyse par des catalyseurs hétérogènes est courante dans de nombreux domaines, notamment la production de produits chimiques, le traitement des eaux usées, la transformation des polluants automobiles et certaines réactions organiques.
Le procédé Harber est un processus de catalyse qui utilise un catalyseur hétérogène solide à base de fer pour produire de l’ammoniac |(\text{NH}_3)| à partir de dihydrogène |(\text{H}_2)| et de diazote |(\text{N}_2).|
||3\ \text{H}_{2\text{(g)}} + \text{N}_{2\text{(g)}} \rightarrow 2\ \text{NH}_{3\text{(g)}}||
Le catalyseur à base de fer est hétérogène, car il est à l’état solide, alors que les réactifs sont à l’état gazeux. L’utilisation de ce catalyseur permet de produire rapidement une grande quantité d’ammoniac. De plus, le même catalyseur peut être réutilisé en permanence.
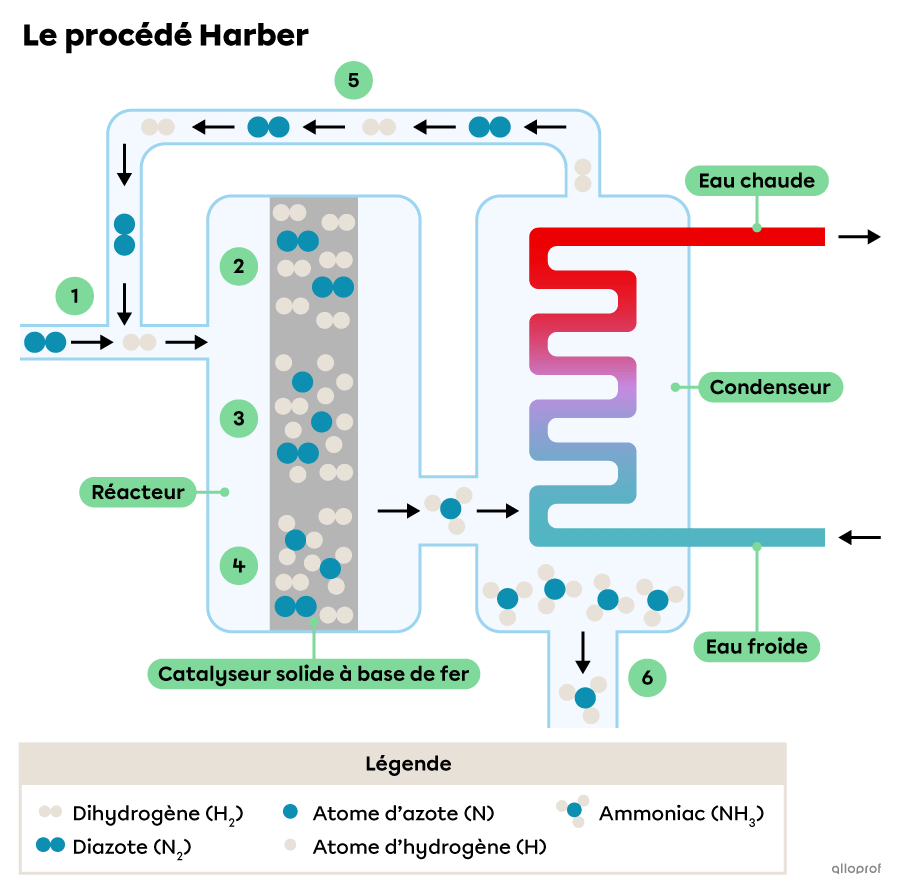
Voici un schéma simplifié du procédé Haber.
Dans ce schéma :
-
Le dihydrogène |(\text{H}_2)| et le diazote |(\text{N}_2)| sont introduits dans le réacteur.
-
Le catalyseur à l’intérieur du réacteur fournit une surface pour l’absorption des molécules de |\text{H}_2| et de |\text{N}_2.|
-
Le catalyseur affaiblit les liaisons chimiques au sein des molécules, ce qui leur permet de se séparer en atomes d’hydrogène |(\text{H})| et d’azote |\text{N}.| Les atomes se diffusent le long de la surface du catalyseur.
-
De nouvelles liaisons se forment entre certains des atomes |\text{H}| et |\text{N}| et des molécules d’ammoniac |(\text{NH}_3)| se forment. L’ammoniac gazeux est libéré de la surface du catalyseur.
-
Les molécules de |\text{H}_2| et de |\text{N}_2| qui n’ont pas réagi sont recueillies et utilisées à nouveau comme réactifs.
-
L’ammoniac gazeux est condensé en ammoniac liquide par le condenseur.
Un catalyseur homogène est un catalyseur qui est utilisé dans le même état que celui des réactifs.
Les catalyseurs homogènes catalysent généralement des réactions où les réactifs sont en solution. La catalyse par catalyseurs homogènes est utilisée dans de nombreux domaines, notamment la recherche pharmaceutique et médicale, le développement de biocarburants et la dégradation des polluants.
L’amincissement de la couche d’ozone |(\text{O}_3)| dans l’atmosphère est catalysée par la présence de chlore |(\text{Cl})| à l’état gazeux. Puisque |\text{O}_3| et |\text{Cl}| sont à l’état gazeux, |\text{Cl}| est donc un catalyseur homogène. La réaction catalysée se produit selon le mécanisme réactionnel suivant.
Étape 1 : |O_{3\text{(g)}} + \color{#EC0000}{Cl_{\text{(g)}}} \rightarrow O_{2\text{(g)}} + \color{#333FB1}{ClO_{\text{(g)}}}|
Étape 2 : |O_{3\text{(g)}} + \color{#333FB1}{ClO_{\text{(g)}}} \rightarrow 2\ O_{2\text{(g)}} + \color{#EC0000}{Cl_{\text{(g)}}}|
Réaction globale : |2\ O_{3\text{(g)}} + \cancel{\color{#EC0000}{Cl_{\text{(g)}}}} + \cancel{\color{#333FB1}{ClO_{\text{(g)}}}} \rightarrow O_{2\text{(g)}} + \cancel{\color{#333FB1}{ClO_{\text{(g)}}}} + 2\ O_{2\text{(g)}} + \cancel{\color{#EC0000}{Cl_{\text{(g)}}}} \\\\ \Rightarrow 2\ O_{3\text{(g)}} \rightarrow 3\ O_{2\text{(g)}}|
On remarque que le catalyseur |\color{#EC0000}{Cl_{\text{(g)}}}| peut être identifié parce qu’il est consommé à l’étape 1 et régénéré à l’étape 2. De plus, il est absent de la réaction globale.
Les enzymes
Une enzyme, également appelée biocatalyseur, est une protéine qui catalyse une réaction biochimique spécifique.
Les enzymes sont des protéines spécifiques qui accélèrent les réactions biochimiques dans les organismes vivants. En tant que catalyseurs homogènes, elles sont impliquées dans les processus digestifs, la réplication de l’ADN, la photosynthèse, la réponse immunitaire et presque tous les autres processus nécessaires à la survie d’un organisme. On estime que les cellules humaines contiennent plus de 3 000 types d’enzymes, chacune catalysant une réaction chimique spécifique.
Plusieurs modèles ont été développés pour tenter d’expliquer le fonctionnement des enzymes. Par exemple, le modèle clé et serrure propose qu’une enzyme a un emplacement spécifique dont la forme et les propriétés chimiques sont uniques. Cet emplacement est appelé site actif. Il ne peut s’associer qu’à un réactif ou à un groupe de réactifs spécifiques, appelé substrat. Les enzymes sont sensibles à la concentration du substrat, ainsi qu’à la température et au pH de l’environnement.
Les enzymes peuvent être synthétisées et utilisées dans le cadre de certains traitements médicaux. En outre, des inhibiteurs peuvent être utilisés pour ralentir l’activité enzymatique naturellement présente dans l’organisme. De nouvelles applications enzymatiques, telles que la biodégradation des plastiques, sont également étudiées par les scientifiques.
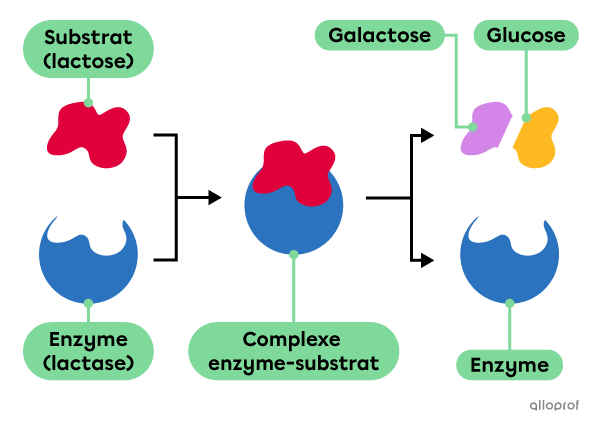
La lactase est une enzyme qui catalyse la digestion du lactose, un sucre présent dans de nombreux produits laitiers. Le lactose est le substrat de la lactase. Normalement, la lactase produite dans l’intestin grêle décompose le lactose en deux sucres simples : le galactose et le glucose.
Des mutations peuvent entrainer la production de molécules de lactase défectueuses et une diminution de l’activité du gène chez l’adulte peut entrainer une diminution de la lactase dans le système digestif. Par conséquent, le lactose ne peut pas subir la digestion chimique et une condition connue sous le nom d’intolérance au lactose peut se développer. Sur recommandation d’un professionnel de la santé, des suppléments de lactase peuvent être ingérés pour catalyser la digestion du lactose.
Les extrêmophiles sont des micro-organismes adaptés pour survivre dans des conditions extrêmes de pH, de température, de salinité, de pression, de radiations ainsi qu’en présence de stress oxydatif, de métaux lourds, de produits chimiques toxiques et qu’en absence d’eau.
Leurs enzymes, connues sous le nom d’extrémozymes, sont capables de catalyser des réactions chimiques dans des conditions extrêmement difficiles. Les chercheurs s’intéressent à l’utilisation des extrémozymes dans les processus industriels agressifs et dans l’industrie alimentaire, afin d’augmenter la vitesse de réaction et de réduire les couts de production.
Deinococcus radiodurans est une bactérie extrêmophile étudiée par les astrobiologistes en raison de sa résistance à des niveaux extrêmes de rayonnements ionisants, y compris les rayons UV et gamma, ainsi qu’à des conditions extrêmement sèches, froides et acides. En fait, selon des recherches récentes, des échantillons de Deinococcus radiodurans ont survécu après avoir été placés à l’extérieur de la station spatiale internationale pendant un an[1].
Source : Life in the Extreme: Radiation [Image en ligne]. Astrobiology at NASA, (10 février 2023). Tous droits réservés*[2]
-
Ott, E., Kawaguchi, Y., Kölbl, D., Rabbow, E., Rettberg, P., Mora, M., Moissl-Eichinger, C., Weckwerth, W., Yamagishi, A., & Milojevic, T. (2020). Molecular repertoire of Deinococcus radiodurans after 1 year of exposure outside the International Space Station within the Tanpopo mission. Microbiome, 8(150). https://doi.org/10.1186/s40168-020-00927-5
-
Life in the Extreme: Radiation [Image en ligne]. Astrobiology at NASA, (10 février 2023). https://astrobiology.nasa.gov/news/life-in-the-extreme-radiation/ *Contenu utilisé par Alloprof en conformité avec la loi sur le droit d’auteur dans le cadre d’une utilisation équitable à des fins éducatives. [https://laws-lois.justice.gc.ca/eng/acts/c-42/page-9.html].