Selon la théorie des collisions, la vitesse d’une réaction chimique est directement proportionnelle au nombre de collisions efficaces entre les particules de réactifs.
En laboratoire, des facteurs peuvent être modifiés afin de faire varier le nombre de collisions efficaces et donc la vitesse de réaction.
Le tableau suivant décrit de manière générale comment certains de ces facteurs influencent la vitesse de réaction.
Clique sur l’un des facteurs pour en voir les détails.
|
Facteur |
Augmentation de la vitesse de réaction |
Diminution de la vitesse de réaction |
|---|---|---|
|
Forte concentration |
Faible concentration |
|
|
Peu de liaisons chimiques à briser |
Grand nombre de liaisons chimiques à briser |
|
|
Liaisons faibles |
Liaisons fortes |
|
|
Énergie cinétique élevée |
Énergie cinétique basse |
|
|
Faible attraction entre les particules |
Forte attraction entre les particules |
|
|
Grande surface de contact |
Petite surface de contact |
|
|
Température élevée |
Température basse |
|
|
Présence d’un catalyseur |
Présence d’un inhibiteur |
En général, une augmentation de la concentration d’un réactif entraine une augmentation de la vitesse de réaction.
En effet, une augmentation du nombre de particules de réactifs dans un volume donné entraine généralement un nombre de collisions plus élevé, ce qui augmente la probabilité qu’il y ait des collisions efficaces.
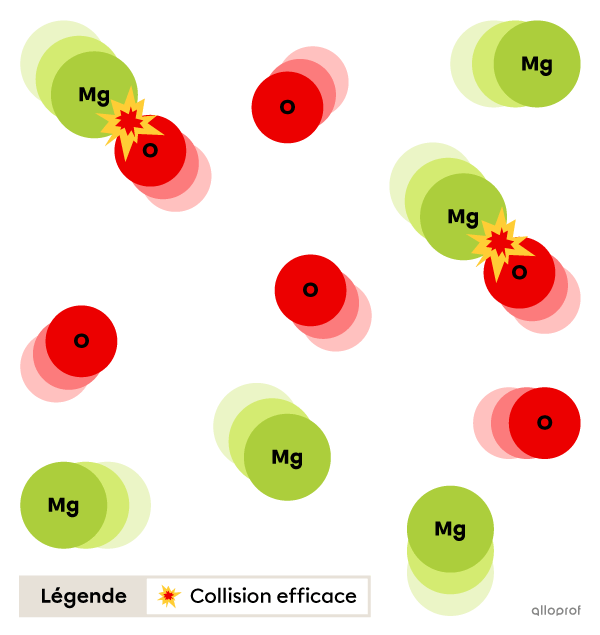
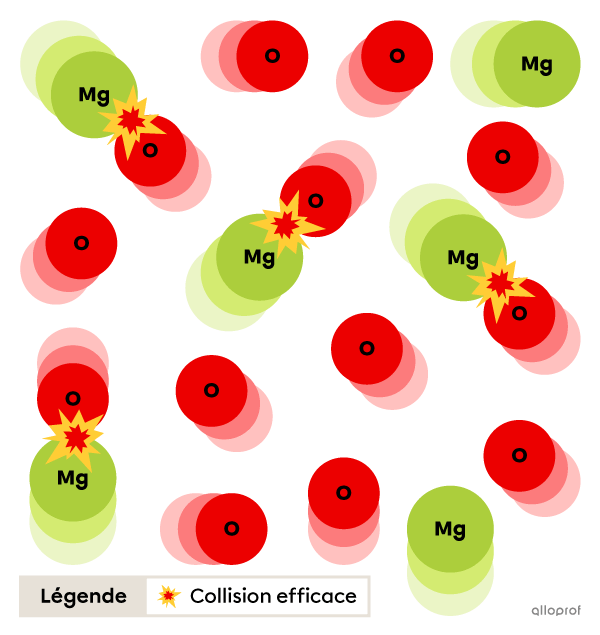
L’effet d’une variation de la concentration d’un réactif sur la vitesse d’une réaction n’est pas toujours directement proportionnel. Par exemple, doubler la concentration des réactifs ne double pas nécessairement la vitesse de réaction. L’effet d’une hausse de concentration des réactifs dépend du type de réaction chimique et de la nature des réactifs.
Pour connaitre précisément l’effet d’une augmentation de la concentration des réactifs sur la vitesse de réaction, on doit utiliser une relation mathématique qui s’appelle la loi des vitesses de réaction.
Le nombre de liaisons à briser, la force des liaisons, la force d’attraction entre les particules et l’énergie cinétique des particules sont tous des facteurs qui influencent l’énergie d’activation. Par le fait même, ils influencent la vitesse de réaction.
Plus l’énergie d’activation est basse, plus la réaction chimique est rapide.
Plus l’énergie d’activation est élevée, plus la réaction chimique est lente.
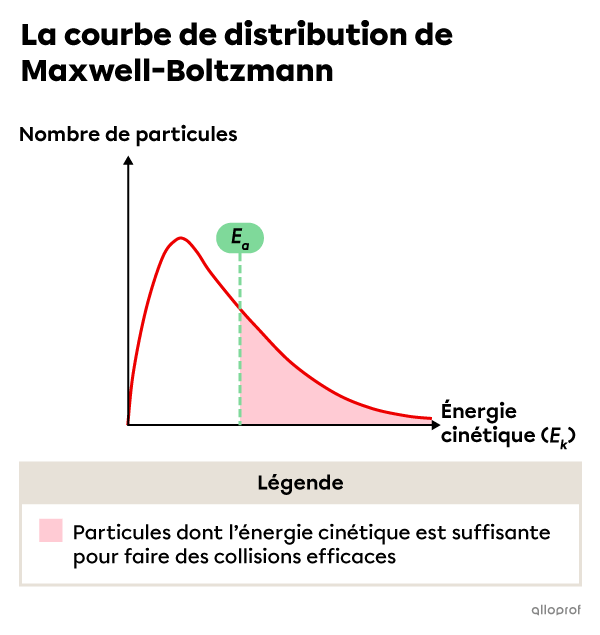
Lorsque l’énergie d’activation |(E_a)| est basse, davantage de particules possèdent l’énergie requise pour faire des collisions efficaces. Plus le nombre de collisions efficaces entre les réactifs est élevé, plus la réaction sera rapide.
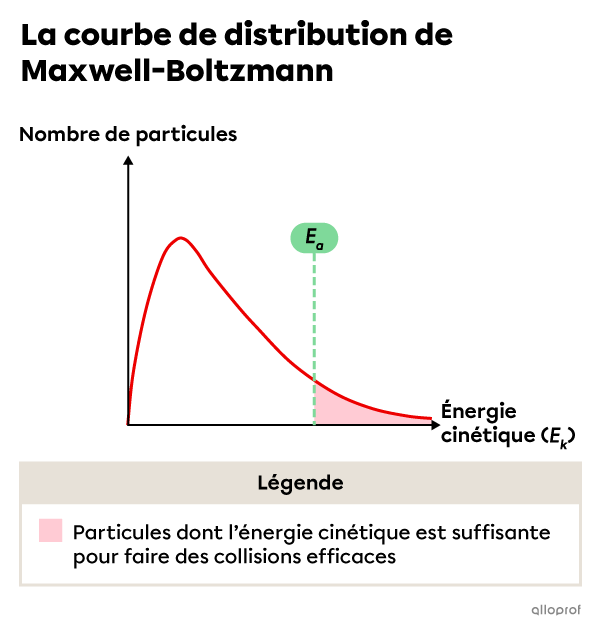
Lorsque l’énergie d’activation |(E_a)| est élevée, moins de particules possèdent l’énergie requise pour faire des collisions efficaces. Moins le nombre de collisions efficaces entre les réactifs est élevé, plus la réaction sera lente.
Le nombre de liaisons chimiques à briser, ainsi que la force des liaisons varient en fonction de la nature des réactifs impliqués dans une réaction chimique.
Le nombre de liaisons chimiques à briser
Lorsqu’on compare des molécules semblables, plus il y a de liaisons chimiques à briser dans les réactifs, plus l’énergie d’activation est élevée. Ainsi, la vitesse de réaction est plus lente.
Dans des conditions de réaction semblables, la combustion du propane |(\text{C}_3\text{H}_8)| est plus lente que celle du méthane |(\text{CH}_4).| En effet, le nombre de liaisons à briser est plus grand dans une molécule de |\text{C}_3\text{H}_8| que dans une molécule de |\text{CH}_4.|
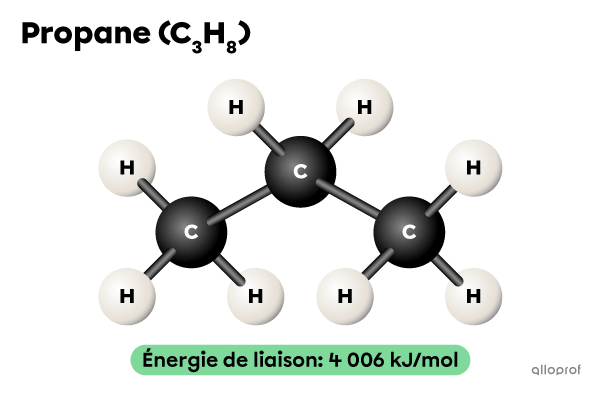
Réaction plus lente
Il faut fournir au minimum |4\ 006\ \text{kJ}| d’énergie pour briser les 10 liaisons chimiques de chaque molécule d’une mole de |\text{C}_3\text{H}_8.|
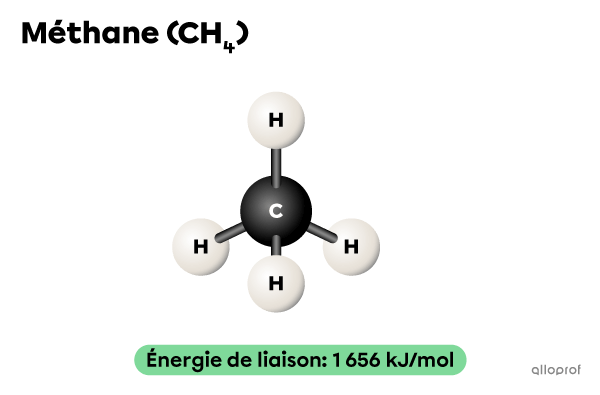
Réaction plus rapide
Il faut fournir |1\ 656\ \text{kJ}| d’énergie pour briser les 4 liaisons chimiques présentes dans chaque molécule d’une mole de |\text{CH}_4.|
La force des liaisons chimiques à briser
Plus l’énergie de liaison des réactifs est faible, plus l’énergie d’activation de la réaction est basse et plus la vitesse de réaction est rapide.
L’énergie de liaison du bromure de sodium |(\text{NaBr})| est plus élevée que l’énergie de liaison de l’iodure de sodium |(\text{NaI}).|
Lorsque ces deux composés réagissent avec le chlorométhane |(\text{CH}_3\text{Cl}),| la réaction avec |\text{NaI}| est plus rapide que la réaction avec |\text{NaBr}.|
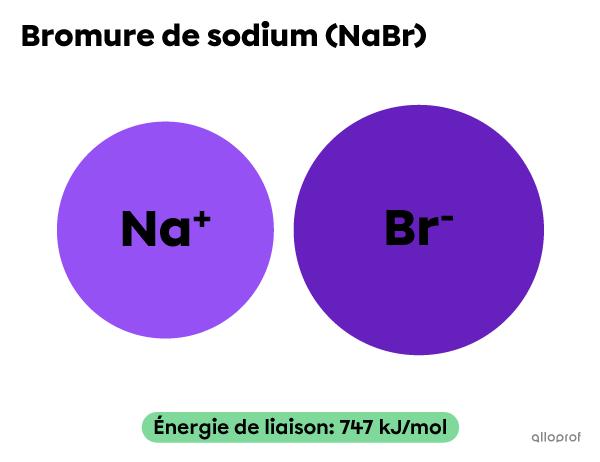
Réaction plus lente
||\text{CH}_3\text{Cl}+\text{NaBr}\rightarrow \text{CH}_3\text{Br}+\text{NaCl}||
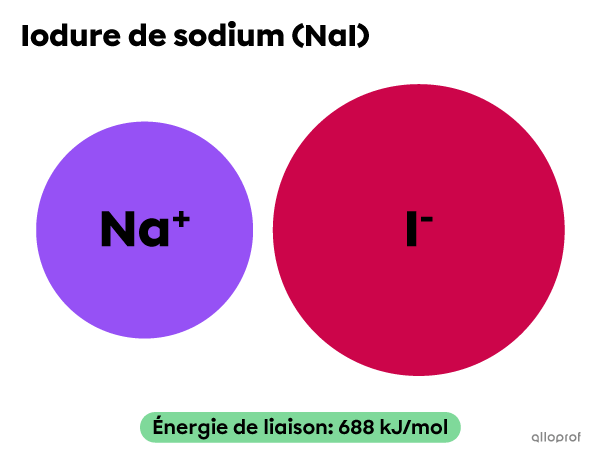
Réaction plus rapide
||\text{CH}_3\text{Cl}+\text{NaI}\rightarrow \text{CH}_3\text{I}+\text{NaCl}||
L’encombrement stérique, ou le facteur stérique, est un phénomène où la disposition des atomes dans un composé rend difficilement accessibles certains atomes. Ces atomes font donc moins de collisions, ce qui réduit le nombre de collisions efficaces et ralentit la réaction.
Par conséquent, même si les réactifs ont peu de liaisons ou des liaisons faibles, il arrive qu’une réaction soit plus lente qu’attendu en raison de l’encombrement stérique.
La force d’attraction entre les particules d’une substance ainsi que l’énergie cinétique des particules varient en fonction de l’état physique de cette substance.
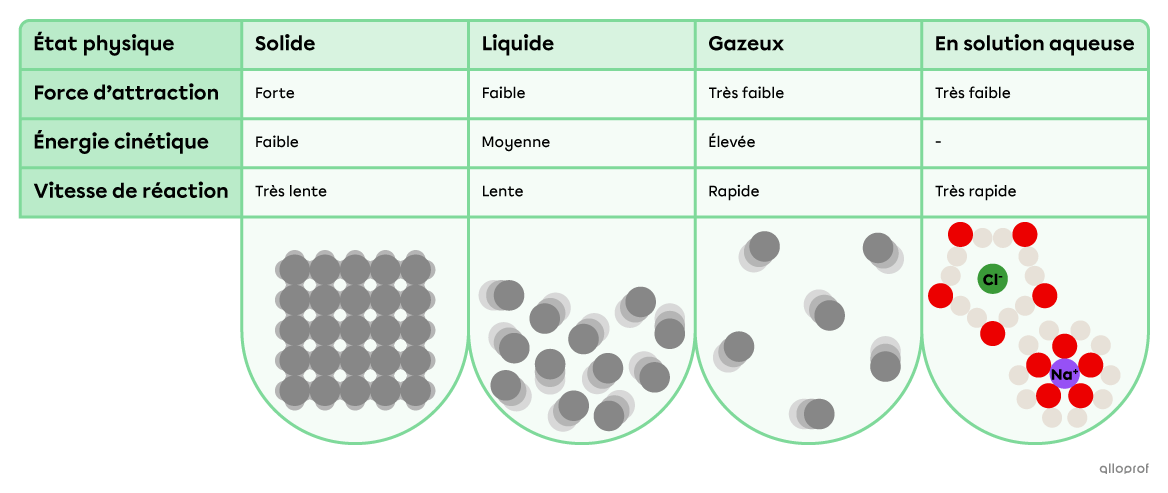
La force d’attraction entre les particules
Plus les forces d’attraction entre les particules de réactifs sont fortes, plus la quantité d’énergie nécessaire pour briser ces forces sera importante, plus l’énergie d’activation de la réaction sera élevée et plus la vitesse de réaction sera lente.
Selon le modèle particulaire, les forces d’attraction sont plus grandes entre les particules d’une substance solide qu’entre les particules de cette même substance à l’état liquide ou à l’état gazeux. De plus, lorsqu’un composé ionique est dissocié en solution, les forces d’attraction entre les ions sont significativement réduites.
L’énergie cinétique des particules
Les particules dont l’énergie cinétique est élevée ont plus de chances d’atteindre un niveau d’énergie supérieur ou égal à l’énergie d’activation |(E_a)| de la réaction.
Selon le modèle particulaire, l’état physique d’une substance influence l’énergie cinétique de ses particules.
-
À l’état solide, l’énergie cinétique des particules est très faible. En effet, les particules d’un solide font uniquement un mouvement de vibration sur place.
-
À l’état liquide, l’énergie cinétique des particules est faible. En effet, tout en demeurant très rapprochées, les particules d’un liquide peuvent glisser les unes par rapport aux autres.
-
À l’état gazeux, l’énergie cinétique des particules est très élevée. En effet, les particules d’un gaz peuvent se déplacer à grande vitesse dans toutes les directions de manière aléatoire.
-
Une réaction homogène est une réaction chimique où tous les réactifs sont dans un même état physique.
-
Une réaction hétérogène est une réaction chimique où tous les réactifs ne sont pas dans un même état physique.
Les réactions homogènes sont généralement plus rapides que les réactions hétérogènes.
Par exemple, la combustion du propane, qui est une réaction homogène où toutes les substances sont gazeuses, est beaucoup plus rapide que la combustion du bois qui est une réaction hétérogène.
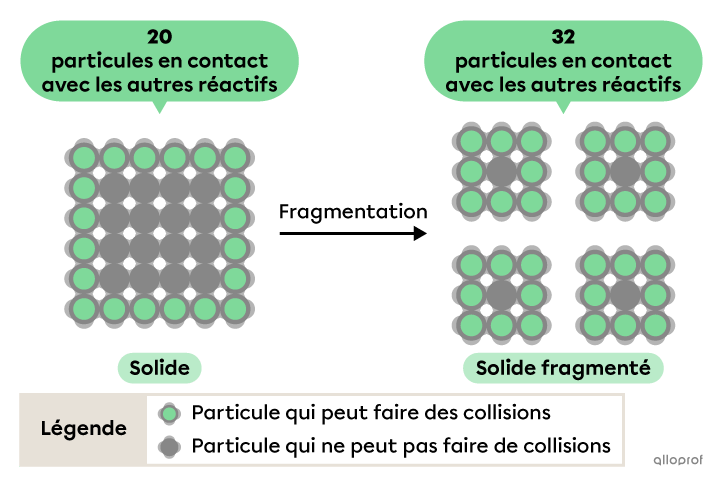
Lorsque l’un des réactifs est à l’état solide, seules les particules à la surface du solide peuvent entrer en contact avec les particules des autres réactifs. Fragmenter un réactif solide permet d’augmenter sa surface de contact avec les autres réactifs, ce qui expose davantage ses particules aux collisions. En permettant un plus grand nombre de collisions, le nombre de collisions efficaces augmente également, ce qui augmente la vitesse de réaction.
Selon la théorie des collisions, la vitesse d’une réaction chimique dépend, entre autres, de l’énergie cinétique des particules de réactifs.
La température est un indice du degré d’agitation des particules. Augmenter la température du milieu réactionnel permet donc d’augmenter l’énergie cinétique des particules de réactifs, ce qui tend à augmenter le nombre de collisions efficaces et la vitesse de réaction.
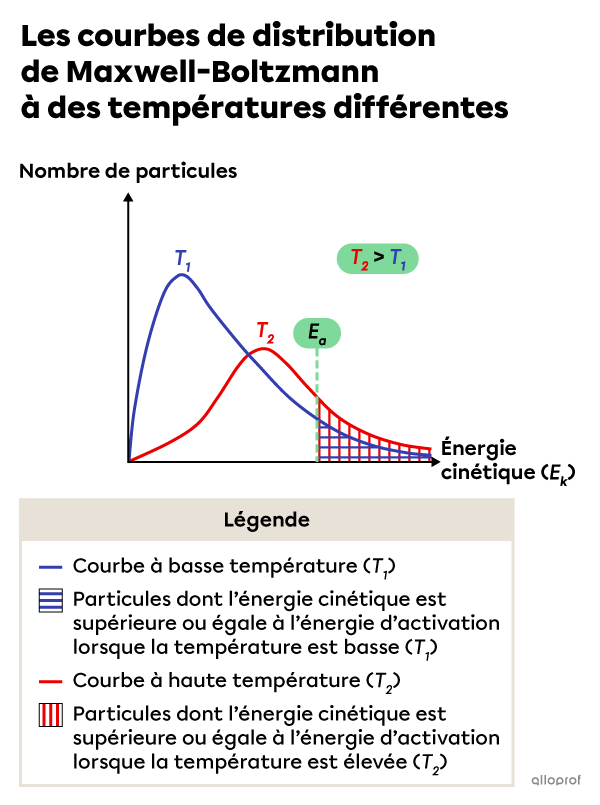
La courbe de distribution de Maxwell-Boltzmann permet de visualiser l’énergie cinétique des particules de réactifs lorsqu’on fait varier la température du milieu réactionnel.
On constate que lorsque la température du milieu réactionnel est plus élevée, un plus grand nombre de particules de réactifs ont une énergie cinétique égale ou supérieure à l’énergie d'activation |(E_a)| de la réaction.
Le réfrigérateur permet d’abaisser la température des aliments afin de ralentir les réactions de fermentation et d’oxydation de certains aliments.

Source : Andrey_Popov, Shutterstock.com
-
Un catalyseur est une substance qui augmente la vitesse d’une réaction chimique en diminuant son énergie d’'activation, sans être consumée dans le processus.
-
Un inhibiteur a l’effet inverse d’un catalyseur, c’est-à-dire qu’il diminue la vitesse d’une réaction chimique en augmentant son énergie d’activation, sans être consumé dans le processus.
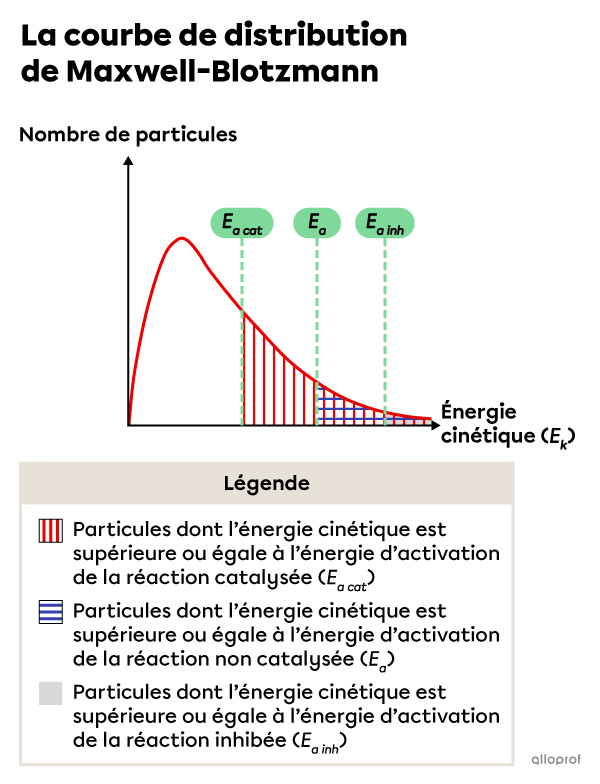
Selon la théorie des collisions, la vitesse d’une réaction est directement proportionnelle au nombre de collisions efficaces.
En abaissant l’énergie d’activation d’une réaction |(E_{a\ cat}),| l’ajout d’un catalyseur permet à un plus grand nombre de particules de réactifs d’atteindre le niveau d’énergie requis pour faire des collisions efficaces. Ainsi, la réaction est plus rapide.
En augmentant l’énergie d’activation d’une réaction |(E_{a\ inh}),| l’ajout d’un inhibiteur permet à un moins grand nombre de particules de réactifs d’atteindre le niveau d’énergie requis pour faire des collisions efficaces. Ainsi, la réaction est plus lente.
Consulte cette fiche notionnelle pour en apprendre davantage sur l’effet des catalyseurs sur la vitesse de réaction et sur les types de catalyseurs.