La séparation des mélanges permet d'isoler ou de séparer certains constituants des mélanges dans lesquels ils se trouvent.
Il est souvent nécessaire, pour obtenir une substance pure, de la séparer de toutes les autres substances qui l'accompagnent. On peut séparer les mélanges par des moyens physiques, qui seront traités dans la présente fiche. Le choix de la technique varie en fonction du mélange, de la substance que l'on doit séparer du reste du mélange et des phases qui constituent le mélange.
Les techniques les plus utilisées sont les suivantes :
L'évaporation est un processus par lequel on élimine la partie liquide d'un mélange en la transformant en gaz.
Pour ce faire, on peut laisser le constituant liquide du mélange s'évaporer naturellement à température ambiante, ou on peut accélérer le processus en chauffant le mélange. L'évaporation sert à récupérer la partie solide d'un mélange hétérogène ou encore le soluté solide d'une solution. Elle permet aussi de concentrer le soluté d'une solution dans un plus petit volume de solvant, comme l'illustre l'image suivante :
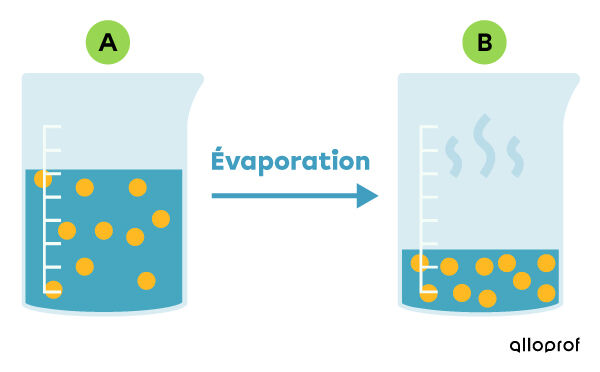
Pour savoir comment pratiquer la technique d’évaporation en laboratoire, consulte la fiche à propos des techniques de séparation des mélanges (laboratoire).
La décantation est un processus qui permet de séparer des substances non miscibles qui n’ont pas la même masse volumique (densité).
Lorsque les constituants à séparer sont liquides, on les laisse reposer dans une ampoule à décantation. Le liquide qui possède la masse volumique la plus grande se déplace alors vers le fond de l’ampoule. Le liquide qui possède la masse volumique la plus petite, quant à lui, se déplace vers le haut. Lorsque les 2 phases sont bien distinctes, on peut séparer les 2 liquides.
Cette technique peut être utilisée pour séparer un mélange d’eau et d’huile. Comme on le remarque sur l’image suivante, l’huile flotte sur l’eau, car l’huile a une masse volumique plus faible que l’eau.
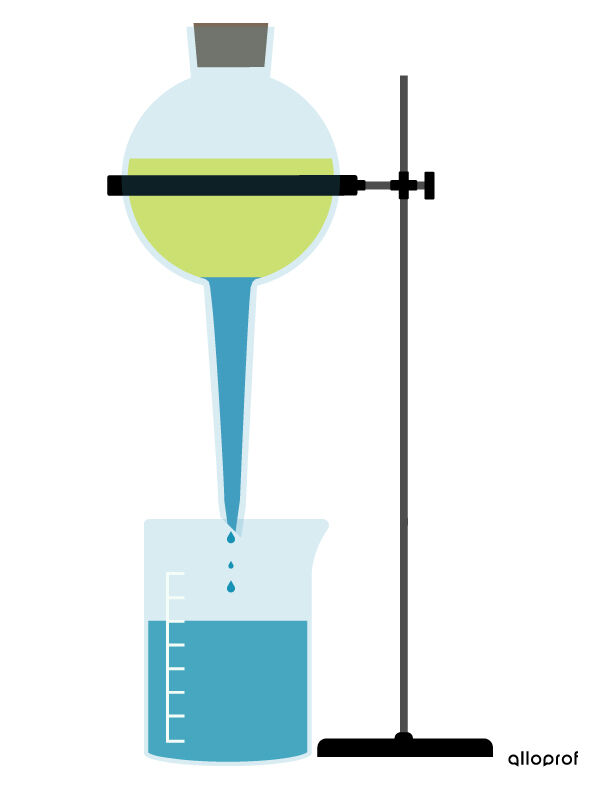
La décantation peut aussi permettre de séparer des particules solides en suspension dans un liquide, ce qui est souvent nommé la sédimentation. Lors de la sédimentation, les particules en suspension cessent de se déplacer et se déposent dans le fond du récipient, sous l’effet de la gravité. Le dépôt est alors appelé sédiment. Une fois que les particules en suspension se sont bien déposées dans le fond du contenant, on utilise une tige de verre pour verser le liquide dans un autre contenant. On se retrouve alors avec le liquide dans un contenant et la partie solide dans un autre contenant.
Cette technique peut être utilisée avec un mélange d’eau et de sable. On laisse le mélange reposer pendant un certain temps. Le sable se dépose alors dans le fond du contenant. On transvide l’eau, à l’aide d’une tige de verre, dans un autre contenant.
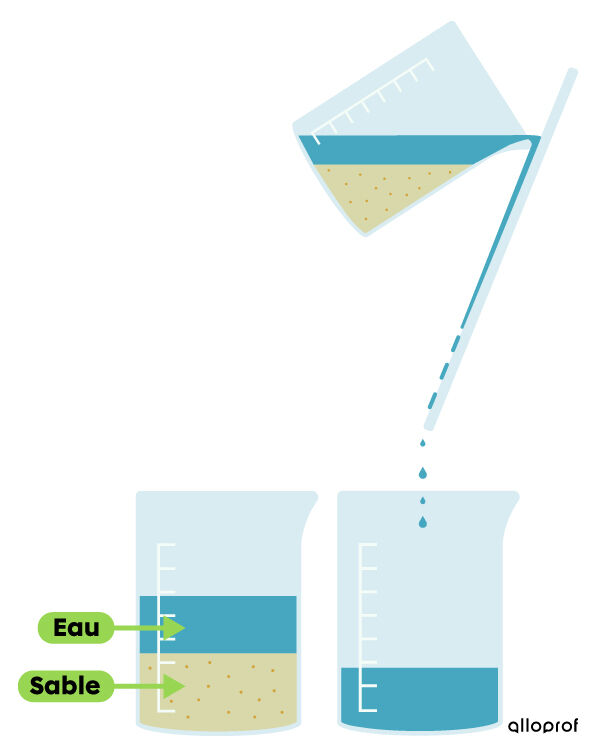
Pour savoir comment pratiquer la technique de décantation en laboratoire, consulte la fiche à propos des techniques de séparation des mélanges (laboratoire).
La filtration est une technique qui permet de séparer les constituants d’un mélange lorsqu’un des constituants est sous la phase liquide et l’autre, sous la phase solide.
Pour ce faire, on utilise un filtre. Ce filtre permet de retenir les particules solides qui sont plus grosses que les pores (trous) du filtre. Le liquide qui passe au travers du filtre est appelé filtrat et le solide qu’on recueille dans le filtre est appelé résidu.
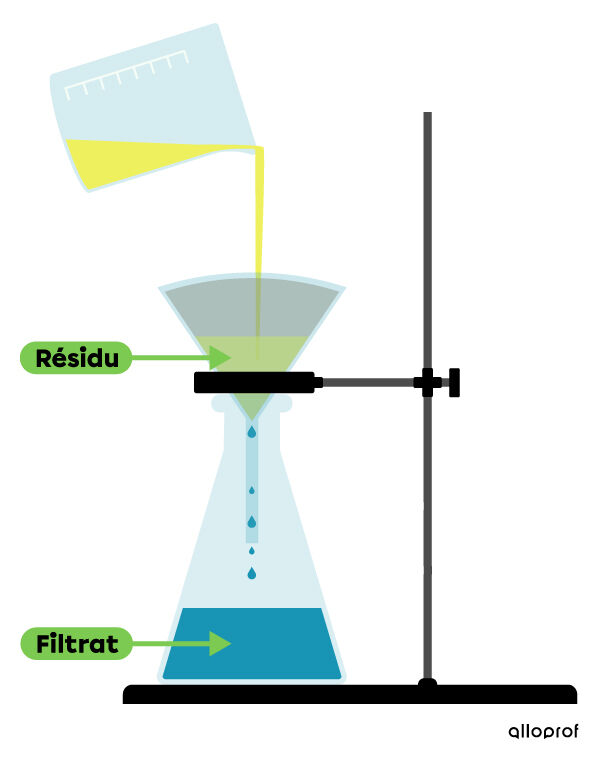
Pour savoir comment pratiquer la technique de la filtration en laboratoire, consulte la fiche à propos des techniques de séparation des mélanges (laboratoire).
La distillation est une technique de séparation des mélanges utilisée pour séparer les constituants d'un mélange homogène liquide ou d'un mélange hétérogène comportant au moins une phase liquide.
En utilisant cette technique, on fait appel à la propriété de point d'ébullition. On chauffe le mélange jusqu’à ce qu'on atteigne le point d’ébullition d’un des constituants. Ce liquide s’évapore alors et la vapeur est recueillie et condensée dans un autre récipient. Pendant que le premier liquide s'évapore (distillat), le deuxième n'atteint pas sa température d'évaporation et reste sous forme liquide dans le contenant initial (résidu).
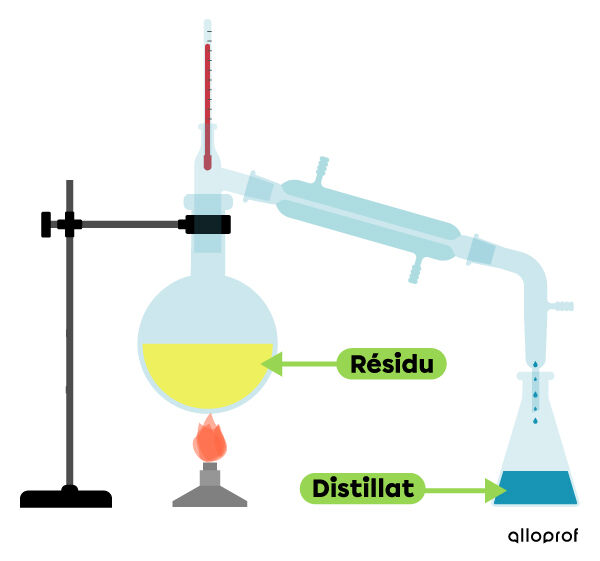
Grâce à cette technique, on peut séparer un mélange d’alcool et d’eau. L’alcool a une température d’ébullition plus basse que l’eau, alors elle s’évapore en premier. La vapeur d’alcool est recueillie et refroidie. Cette condensation permet de récupérer l’alcool (distillat) dans un autre contenant. L’eau (résidu) reste dans le contenant initial.
Pour en savoir davantage sur la technique de la distillation en laboratoire, consulte la fiche à propos des techniques de séparation des mélanges (laboratoire).
La technique du tamisage consiste à séparer les constituants d’un mélange de substances solides à l’aide d’un tamis.
Un tamis est un instrument qui ressemble à un grillage, comme les cordes d’une raquette de tennis. L’espace entre les fils est plus ou moins grand, ce qui permet de laisser passer les particules plus petites du mélange et d’emprisonner les particules plus grosses. Il est alors possible de séparer les constituants du mélange selon la grosseur de ses particules.

Konstantin Kolosov, Shutterstock.com
On peut séparer un mélange de sable fin et de cailloux à l’aide d’un tamis. Il suffit de passer tout le mélange à travers le tamis. Ainsi, les cailloux demeureront sur le tamis et le sable fin passera au travers.
La centrifugation est une technique de séparation qui, par l’action de la force centrifuge, permet de séparer de 2 à 3 phases d'un mélange.
Le mélange est entrainé dans un mouvement de rotation très rapide. Les particules solides les plus lourdes sont alors poussées vers les parois du récipient sous l'action de la force centrifuge, alors que les particules plus légères et les liquides restent en surface, ce qu'on nomme le surnageant. L’appareil qui sert à réaliser une centrifugation est appelé centrifugeuse.
À l’aide d’une centrifugeuse, on peut séparer les globules rouges du plasma sanguin.

Ktsdesign, Shutterstock.com
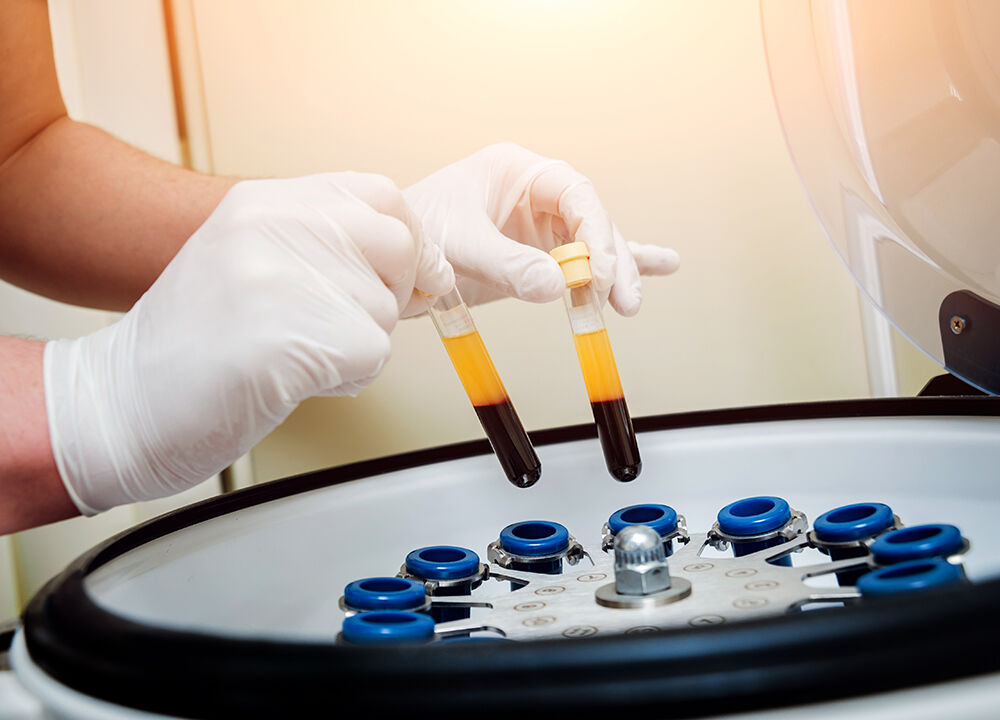
Roman Zaiets, Shutterstock.com
Le principe de fonctionnement est le même que pour une essoreuse à salade. On place la salade dans l’essoreuse et on fait tourner le tout très rapidement. Les feuilles de salade collent à la paroi du panier tandis que l’eau colle à la paroi du récipient. Lorsque tout arrête de tourner, l’eau tombe et elle est récupérée dans le bas du panier.
Pour connaitre comment pratiquer la technique de la centrifugation en laboratoire, consulte la fiche à propos des techniques de séparation des mélanges (laboratoire).
La chromatographie sur papier permet de séparer les constituants d’un mélange grâce à leurs différentes vitesses de migration.
Pour réaliser cette technique, on doit maintenir verticalement des bandes de papier et plonger leur base dans un solvant. Le solvant peut être de l’eau ou de l’alcool. Le mélange qu’on veut séparer est déposé à la base de la bande de papier.
Le liquide monte alors le long de la bande de papier par capillarité et entraine les différents constituants du mélange avec lui.
Chaque constituant est entrainé à une vitesse différente. Les différentes substances se séparent au fur et à mesure sur le papier. Les substances ainsi séparées, bien souvent des molécules, apparaissent finalement sous forme de taches colorées.

Ggw, Shutterstock.com
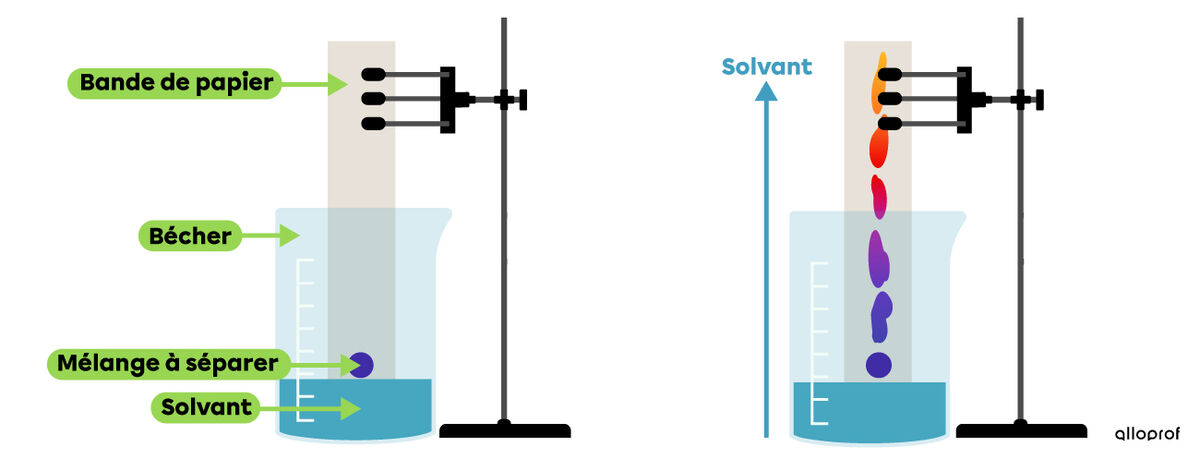
Dans certains cas, on dissout le mélange à séparer directement dans le solvant, plutôt que de le placer sur la bande de papier. Le solvant entraine alors le mélange avec lui en montant dans la bande de papier.
Il existe des techniques plus complexes de séparation des mélanges, qui nécessitent, entre autres, l'ajout de réactifs pour initier une réaction chimique (la précipitation).
La précipitation consiste à former une phase hétérogène au sein d’une autre phase. Si on soupçonne la présence de certains ions dans une solution, il est possible d'ajouter un autre ion qui formera une substance solide avec eux. Ainsi, s’il y a effectivement présence de l’ion recherché, on verra apparaitre une substance solide qu’on pourra par la suite filtrer et récupérer. La précipitation est un moyen chimique de séparation des mélanges.
Si on veut récupérer les ions de plomb dans une solution de nitrate de plomb (|Pb(NO_{3})_{2}|), on peut ajouter une solution contenant de l’iode. Le plomb se lie avec l’iode pour former du iodure de plomb (|PbI_{2}|), qui est un solide poudreux jaune.
