Cette fiche explique les manipulations à suivre pour préparer une solution à une concentration demandée.
Une solution est un mélange composé d'une substance présente en petite quantité, le soluté, dissoute dans une autre substance présente en plus grande quantité, le solvant. Lorsque le solvant est l'eau, on nomme ce mélange solution aqueuse.
Pour préparer ces deux solutions, on peut procéder de deux façons différentes, soit par dissolution ou par dilution.
Dans une dissolution, il faut prendre le soluté et le dissoudre dans le solvant pour obtenir la solution désirée.
Afin de préparer la solution à la concentration demandée, il faut connaître le volume de la solution à préparer et la quantité de soluté nécessaire pour la faire. De manière générale, le volume est déterminé par la fiole jaugée dans laquelle on prépare la solution. Toutefois, la masse n'est généralement pas mentionnée. Il faut donc la calculer avant de débuter les manipulations.
Quelle quantité de soluté faut-il mesurer pour préparer une solution de |\small 12 \: \text {g/L}| dans une fiole jaugée de |\small 100\: \text {ml}| ?
Il faut tout d'abord identifier les variables dans cette situation.
||\begin{align}C &= 12\: \text{g/L} \\ m &=x\: \text{} \\V &=100\: \text{ml} = 0,100\:\text{L}\end{align}||
En utilisant la formule de la concentration, la quantité de soluté à ajouter peut être calculée.
||\begin{align} \displaystyle C=\frac{m}{V} \quad \Rightarrow \quad m &=
C\times V\\ \\
&= \displaystyle 12\: \text{g/L} \times 0,100\:\text{L}\\ \\
&= 1,2 \:\text{g} \end{align}||
Il faudra donc mesurer |1,2 \:\text{g}| de soluté pour préparer cette solution.
- Solide à dissoudre
- Nacelle de pesée
- Spatule
- Balance à fléau
- Eau distillée
- Cylindre gradué
- Fiole jaugée
- Bouchon de caoutchouc
- Tablier ou sarrau
- Lunettes de sécurité

1. Calculer la quantité de soluté nécessaire pour préparer la solution demandée.
2. À l'aide de la balance, peser la nacelle et noter sa masse.
3. Calculer la masse totale du soluté avec la nacelle.
Si la nacelle a une masse de |\small 2,49 \text { g}|, et que l'on doive ajouter |\small 1,2 \text { g}| de soluté, la masse totale de la nacelle avec le soluté sera calculé de la façon suivante.
|\small 2,49 \text { g} + \small 1,2 \text { g} = \small 3,69 \text { g}|
Il faut donc déplacer les curseurs de la balance à |\small 3,69 \text { g}|. Ceci représentera la masse de la nacelle avec le soluté.
4. À l'aide de la nacelle de pesée et la balance, ajouter le soluté jusqu'à ce que l'aiguille soit alignée avec le zéro de la balance.

<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p><a href="/fr/eleves/bv/sciences/la-mesure-de-la-masse-s1501">La mesure de la masse</a></p>
</body></html>
5. Dans la fiole jaugée, ajouter le solvant afin d'obtenir environ la moitié du volume total de la solution.

Il ne faut pas immédiatement mettre le volume total du solvant dans la fiole jaugée, car la solution finale excédera 100 ml puisque la présence du soluté fait augmenter légèrement le volume de la solution.
6. Verser le soluté dans la fiole jaugée.

7. Agiter jusqu'à dissolution complète.
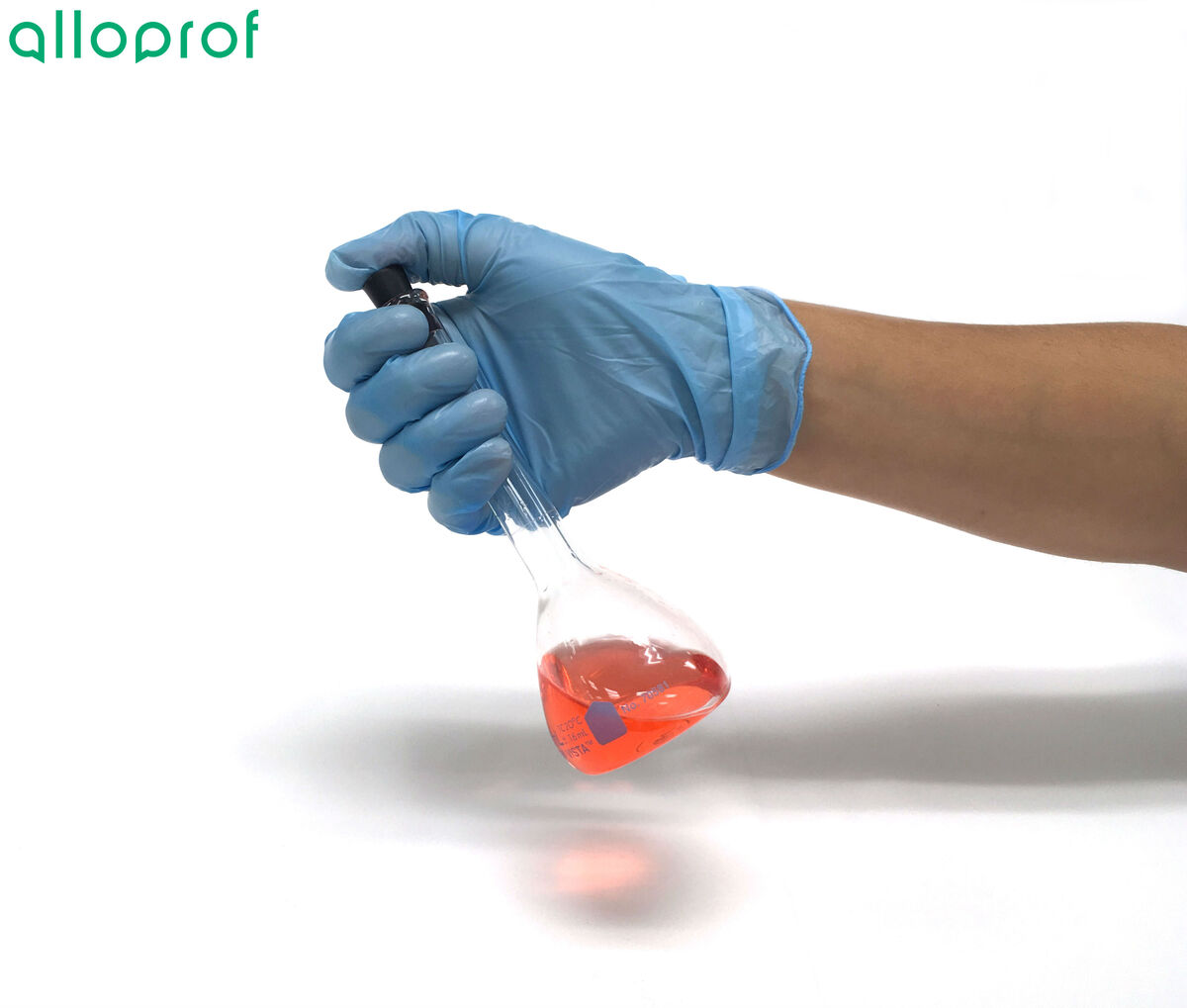
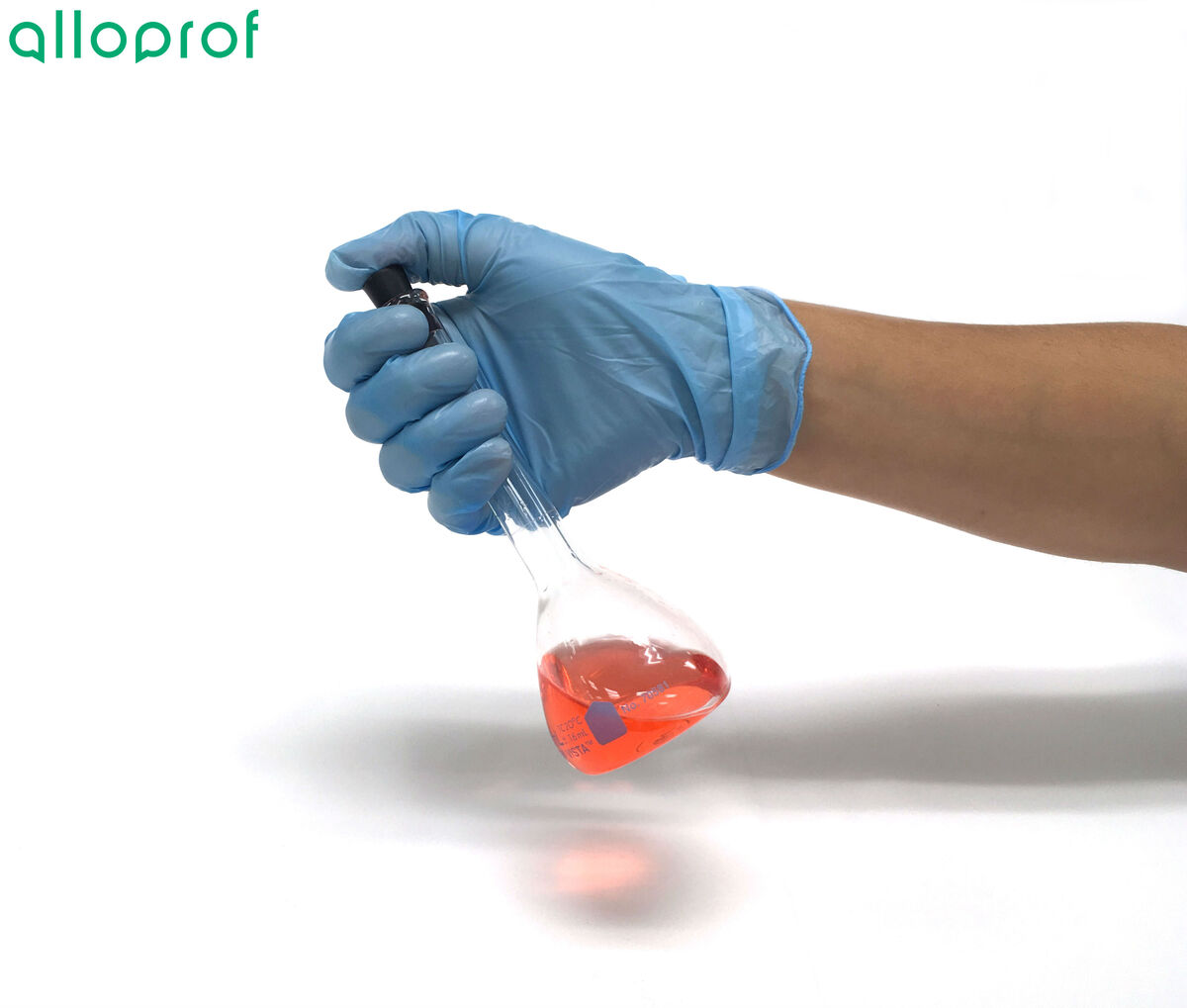
Afin d'éviter que le mélange ne se renverse, il est recommandé de tenir la fiole jaugée par la partie supérieure en plaçant le pouce sur le bouchon. Ceci permettra d'assurer une meilleure étanchéité du bouchon sur la fiole jaugée.

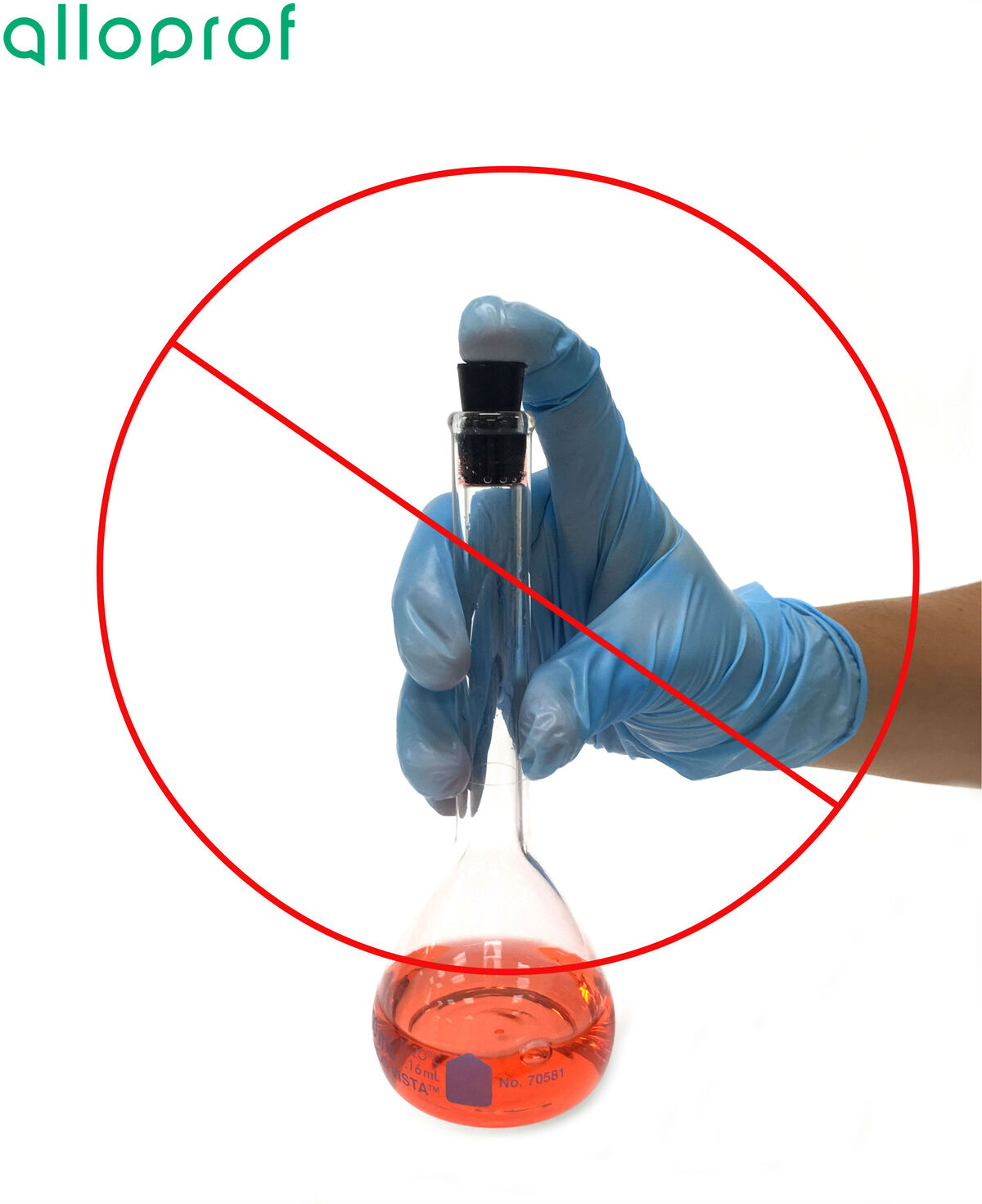
Si le soluté ne s'est pas complètement dissout, il faut ajouter un peu de solvant sans dépasser le volume maximal et agiter à nouveau.
8. Ajouter du solvant jusqu'à l'obtention du volume total de solution maximal. L'utilisation du compte-gouttes peut être considérée afin d'obtenir plus facilement la précision voulue.

9. Agiter à nouveau.
10. Nettoyer et ranger le matériel.
Les calculs ont déjà été faits au début de l'expérience. Il faudrait donc présenter les données expérimentales sous forme de tableau des résultats.
Préparation d'une solution par dissolution
| | Solution |
| |m| | |\text {1,2 g}| |
| |V| | |\text {0,100 L}| |
| |C| | |\text {12 g/L}| |
La solution préparée peut être ensuite utilisée dans une autre expérience. Dans certains cas, pour vérifier la qualité de la préparation effectuée, il peut être demandé de procéder à une analyse par colorimétrie ou de comparer avec des témoins afin de s'assurer que la concentration préparée est la bonne.
Dans une dilution, il faut prendre la solution et y ajouter du solvant afin d'en réduire la concentration.
Pour préparer une solution diluée, il faut tout d'abord déterminer quelle quantité de la solution initiale sera utilisée pour préparer la nouvelle solution diluée. Pour ce faire, il faut connaître les concentrations initiales et finales des solutions ainsi que le volume final de la nouvelle solution.
Quelle quantité d'une solution initiale dont la concentration est |\small 100 \: \text {g/L}| faut-il mesurer pour préparer une solution de concentration |\small 20 \: \text {g/L}| dans une fiole jaugée de |\small 250 \: \text {ml}| ?
Il faut tout d'abord identifier les variables dans cette situation.
||\begin{align}C_{1} &= 100\: \text{g/L} & &\quad & C_{2} &= 20\:\text{g/L}\\
V_{1} &= x & & & V_{2} &= \: 250 \: \text{ml} \:= \: 0,250 \: \text{L}\\
\end{align}||
En utilisant la formule de la concentration, la quantité de soluté à ajouter peut être calculée.
||\begin{align} C_1\times V_1=C_2\times V_2 \quad \Rightarrow \quad V_1 &=\displaystyle\frac{C_2 \times V_2}{C_1}
\\ \\
&= \displaystyle\frac{20\: \text{g/L} \times 0,250 \:\text{L}}{100\: \text{g/L}}\\ \\
&= 0,05 \:\text{L} = 50 \:\text{ml}\end{align}||
Il faudra donc mesurer |50 \:\text{ml}| de la solution initiale à |\small 100 \: \text {g/L}| pour préparer cette solution.
- Solution initiale
- Cylindre gradué
- Eau distillée
- Fiole jaugée
- Bouchon de caoutchouc
- Tablier ou sarrau
- Lunettes de sécurité

1. Calculer la quantité de solution initiale nécessaire pour préparer la solution demandée.
2. Mesurer la quantité calculée à l'étape précédente à l'aide d'un cylindre gradué.

3. Verser le volume mesuré à la deuxième étape dans la fiole jaugée.

4. Ajouter du solvant jusqu'à l'obtention du volume total de solution maximal. L'utilisation du compte-gouttes peut être considérée afin d'obtenir plus facilement la précision voulue.

<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p><a href="/fr/eleves/bv/sciences/la-mesure-du-volume-s1502#liquide">La lecture du volume</a></p>
</body></html>
5. Agiter pour rendre le mélange homogène.

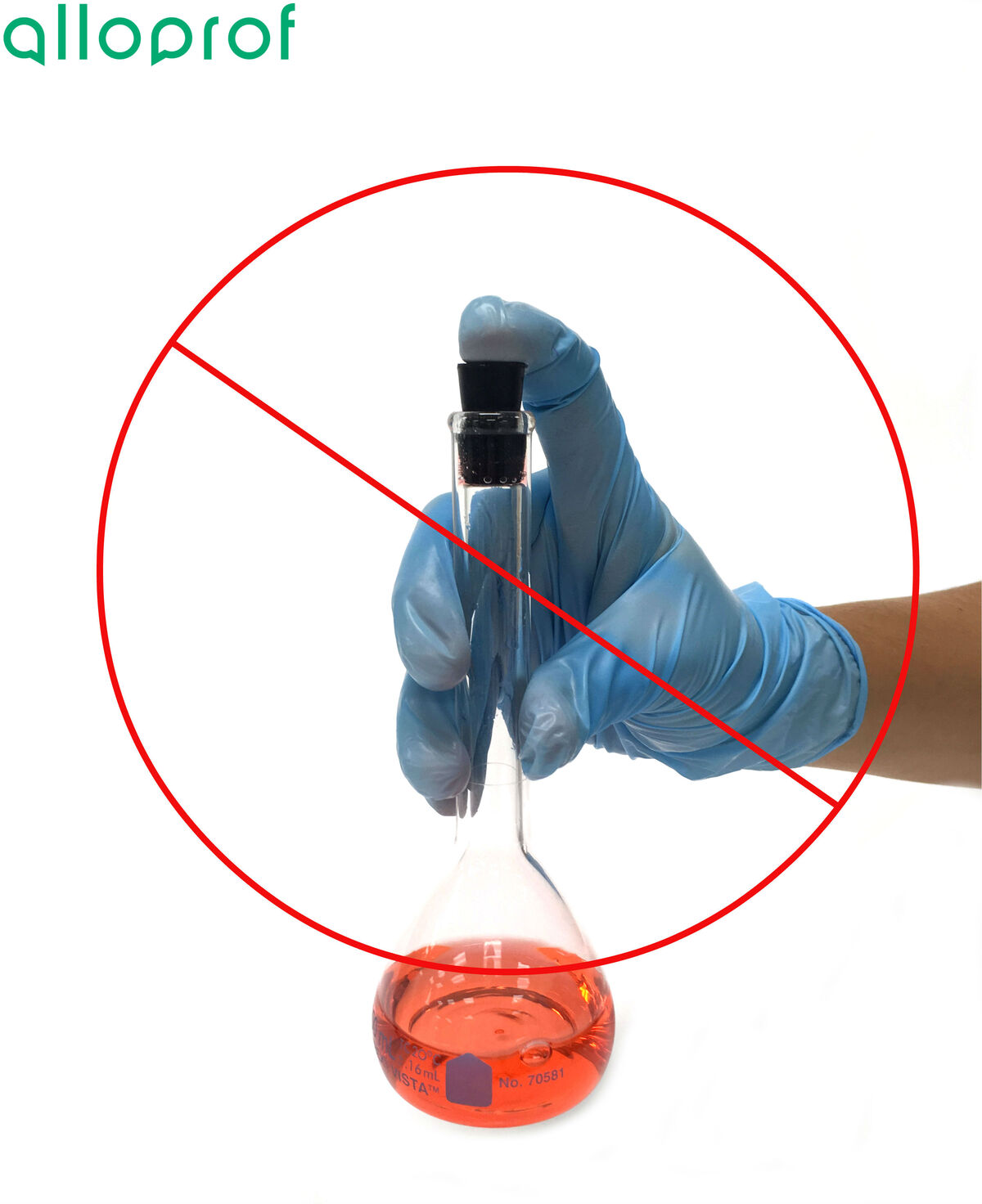
Afin d'éviter que le mélange ne se renverse, il est recommandé de tenir la fiole jaugée par la partie supérieure en plaçant le pouce sur le bouchon. Ceci permettra d'assurer une meilleure étanchéité du bouchon sur la fiole jaugée.

6. Nettoyer et ranger le matériel.
Les calculs ont déjà été faits avant de commencer l'expérience. Il suffit donc de présenter les valeurs importantes du laboratoire sous forme de tableau des résultats.
Préparation d'une solution par dilution
| | Solution |
| |C_1| | |100 \text {g/L}| |
| |V_1| | |\text {0,050 L ou 50 ml}| |
| |C_2| | |\text {20 g/L}| |
| |V_2| | |\text {0,250 L ou 250 ml}| |
La colorimétrie ou la comparaison avec des témoins sont deux techniques qui peuvent être utilisées pour valider la qualité de la démarche.
<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p><a href="/fr/eleves/bv/sciences/la-dilution-c1v1-c2v2-s1054">La dilution</a></p>
</body></html>