La dissolution est un procédé qui consiste à mettre un soluté dans un solvant dans le but de préparer une solution constituée d’une seule phase (mélange homogène).
Lorsqu'on mélange un soluté et un solvant, les molécules de soluté se déplacent jusqu'à ce qu'elles soient réparties de manière uniforme dans l'eau. Les molécules du soluté et du solvant resteront les mêmes: il s'agit donc du même soluté et du même solvant que ceux présents au départ.
Lorsqu'on ajoute du sucre dans un café, les molécules de sucre viendront se placer entre les molécules du solvant, soit l'eau.

Lorsqu’on ajoute trop de soluté à dissoudre dans un solvant, il est possible qu’une partie du soluté n’arrive plus à se dissoudre. On dit alors de cette solution qu’elle est saturée.
On utilise souvent l'eau comme solvant. Lorsqu'on dissout un soluté dans l'eau, le mélange obtenu est une solution aqueuse.
Il existe certains facteurs qui peuvent faire varier la quantité de soluté pouvant être dissoute dans un solvant. Lorsque la température du solvant augmente, il est possible de dissoudre une plus grande quantité de soluté que si la température est plus faible. De plus, la nature du soluté influence la dissolution: pour un même volume d'eau, il n'est pas possible de dissoudre la même quantité de soluté avant d'obtenir une solution saturée. La quantité de soluté pouvant être dissoute dans un volume déterminé d'eau représente la solubilitéde cette substance.
La concentration permet de savoir la quantité de soluté qui a été dissoute dans un volume de solution. Les fiches suivantes expliquent comment calculer la concentration d'une substance.
La concentration et ses unités de mesure
Les ppm (parties par million)
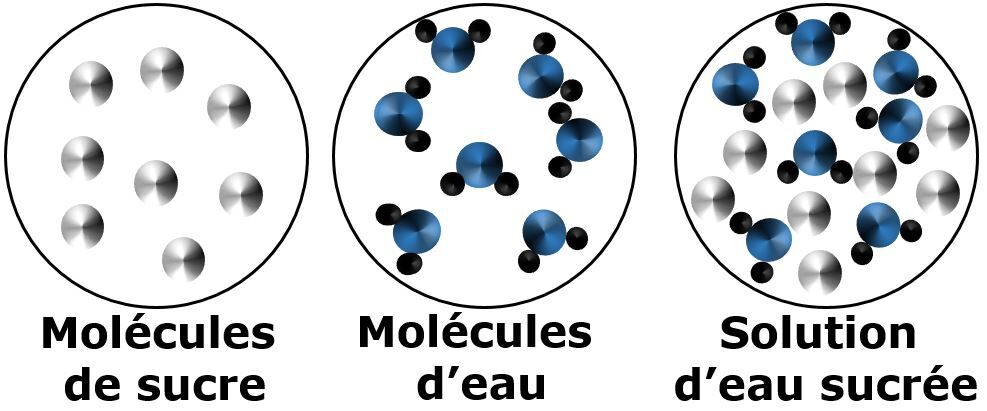
Lors de la dissolution moléculaire, les molécules dissoutes demeurent entières et ne se séparent pas en ions. Étant donné qu’il n’y a pas d’ion, ce type de solution ne conduit pas l’électricité.
Les liens entre les atomes de la molécule du soluté et celles du solvant ne se défont pas.
Lorsque du sucre est dissous dans l'eau, les molécules du soluté vont se mélanger à celle de l'eau sans se défaire.
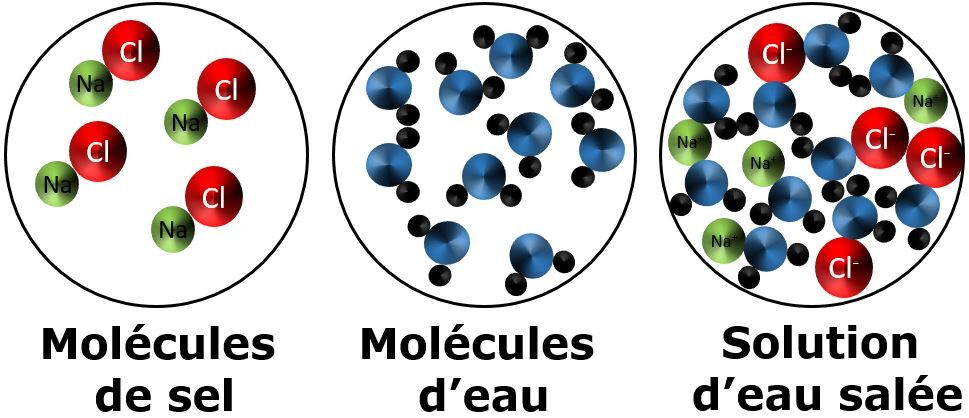
Une dissolution ionique est le résultat du mélange d'un solvant et d'un soluté qui se sépare en ions. Ce type de solution conduit donc l’électricité.
Lorsque du sel de table |(NaCl)| est dissous dans l'eau, le sel se dissocie et produit deux ions, |Na^{+}| et |Cl^{-}|. La solution d'eau salée est donc un électrolyte, soit une solution qui permet le passage du courant électrique.