Une neutralisation acidobasique est une réaction entre un acide et une base au cours de laquelle se forment un sel et de l'eau.
L'équation générale d'une neutralisation acidobasique est la suivante:
|\color{red} {\text {Acide}} + \color{blue} {\text {Base}} \rightarrow {\text {Sel}} + {\text {Eau}}|
Cette réaction peut également être écrite sous la forme suivante:
|\color{red} {\text {H}}{\text {A}} + {\text {B}}\color{blue} {\text {OH}} \rightarrow {\text {BA}} + \color{red} {\text {H}}\color{blue} {\text {OH}}|
Voici quelques exemples de réactions de neutralisation acidobasique.
|\color{red} {HCl} + \color{blue} {NaOH} \rightarrow {NaCl} + {H_{2}O}|
|\color{red} {H_{2}SO_{4}} + \color{blue} {Ba(OH)_{2}} \rightarrow {BaSO_{4}} + 2 {H_{2}O}|
On peut aussi présenter une neutralisation selon le modèle particulaire.
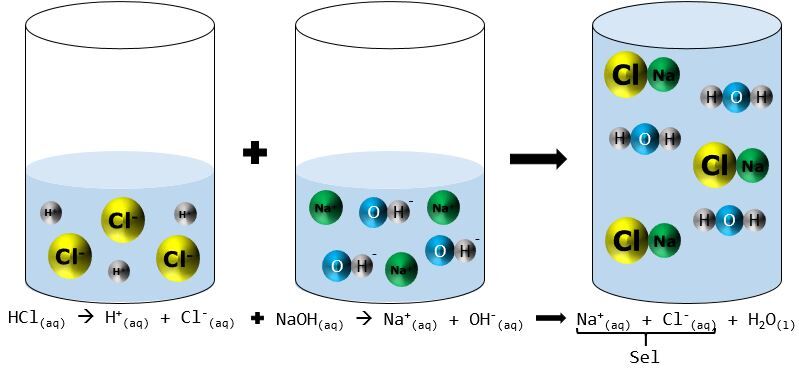
En milieu aqueux, l'acide chlorhydrique |(HCl)| se sépare pour former deux ions, |H^{+}| et |Cl^{-}|. La base, l'hydroxyde de sodium |(NaOH)|, se dissocie également en ions, |Na^{+}| et |OH^{-}|. Lorsqu'on mélange l'acide avec la base, les ions |H^{+}| et |OH^{-}| réagissent ensemble pour former de l'eau. Les deux autres ions, |Na^{+}| et |Cl^{-}|, s'unissent pour former le sel, le chlorure de sodium |(NaCl)|.
En somme, lorsqu’on neutralise une substance, on veut ramener son pH le plus près possible de 7. Les ions |H^{+}| et les ions |OH^{-}| doivent être en même quantité pour que la solution soit dite neutre.
En laboratoire, les principes de la neutralisation acidobasique peuvent être appliqués lors d'un titrage acidobasique afin de déterminer la concentration d'une substance. Ce titrage peut se faire à l'aide d'une burette et d'un indicateur acidobasique. Il faut ajouter quelques gouttes d'indicateur acidobasique dans la solution à neutraliser (l'analyte). Selon la couleur obtenue avec l'indicateur, il faudra neutraliser avec un acide (si la solution est basique) ou avec une base (si la solution est acide). Il faut ensuite ajouter de la solution neutralisante (le titrant) goutte à goutte jusqu'à ce que la solution soit neutralisée, soit jusqu'à ce qu'il y ait autant d'ions |H{+}| que d'ions |OH^{-}|.
Un acide peut être neutralisé par un carbonate comme dans l’exemple qui suit.
|2 HCl + CaCO_{3} \rightarrow CaCl_{2} + H_{2}O + CO_{2}|
Dans cette réaction de neutralisation, il y aura aussi une production de dioxyde de carbone |(CO_{2})|. On pourra donc observer de l’effervescence lors de cette réaction.
Certaines réactions de neutralisation acidobasique sont présentes dans la vie courante. Par exemple, pour neutraliser l'acidité d'un lac ou d'un sol, il faut ajouter de la chaux.
On peut également neutraliser l'acidité du système digestif en utilisant des antiacides.
<!DOCTYPE html PUBLIC "-//W3C//DTD HTML 4.0 Transitional//EN" "http://www.w3.org/TR/REC-html40/loose.dtd">
<html><body><p><span><a href="/fr/eleves/bv/sciences/la-technique-de-neutralisation-d-une-solution-tit-s1509">La technique de neutralisation d'une solution (titrage)</a></span></p>
</body></html>


