Choisis ton niveau.
-
Le pH, abréviation de potentiel hydrogène, est une mesure qui permet de déterminer le degré d’acidité ou de basicité d’une solution. Le pH n’a pas d’unité de mesure.
-
L’échelle de pH permet de comparer le caractère acide, neutre ou basique des solutions. L’échelle de pH varie généralement de 0 à 14.
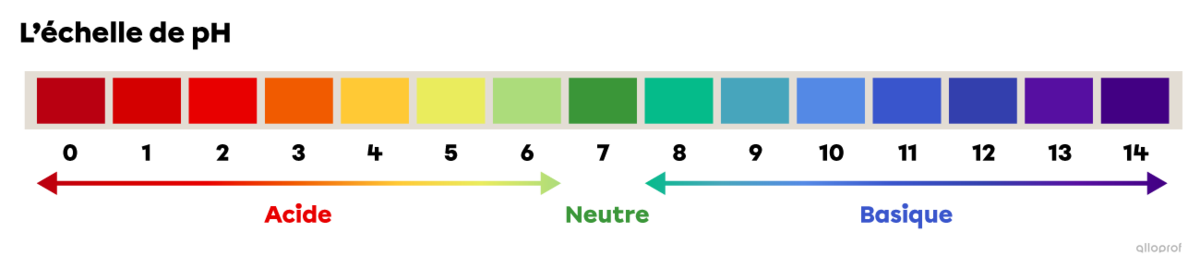
Une solution aqueuse comprend toujours des ions hydrogène |(\text{H}^+)| et des ions hydroxyde |(\text{OH}^-)|. La valeur du pH d’une solution aqueuse dépend de la concentration des ions |\text{H}^+| par rapport à la concentration des ions |\text{OH}^-| présents dans la solution.
-
Lorsque la concentration en ions |\text{H}^+| est plus grande que la concentration en ions |\text{OH}^-,| le pH est plus petit que 7 et la solution est acide.
-
Lorsque la concentration en ions |\text{H}^+| est égale à la concentration en ions |\text{OH}^-,| le pH est égal à 7 et la solution est neutre.
-
Lorsque la concentration en ions |\text{H}^+| est plus petite que la concentration en ions |\text{OH}^-,| le pH est plus grand que 7 et la solution est basique.
Pour évaluer le degré d’acidité ou de basicité d’une solution aqueuse, on peut se servir de l’échelle de pH.
-
Un acide est une substance qui permet la libération d’ions |\text{H}^+| en solution aqueuse.
-
Une base est une substance qui permet la libération d’ions |\text{OH}^-| en solution aqueuse.
-
Le pH, abréviation de potentiel hydrogène, est une mesure qui permet de déterminer le degré d’acidité ou de basicité d’une solution. Le pH n’a pas d’unité de mesure.
-
L’échelle de pH permet de comparer le caractère acide, neutre ou basique des substances. L’échelle de pH varie généralement de 0 à 14.
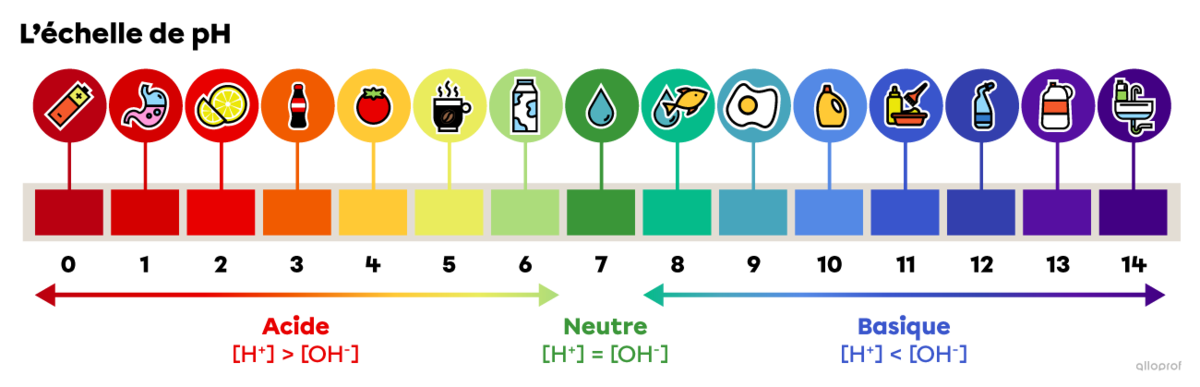
Sur l’échelle de pH, 0 est la valeur la plus acide, 7 est neutre et 14 est la valeur la plus basique. L’image suivante indique le pH approximatif de quelques substances communes.
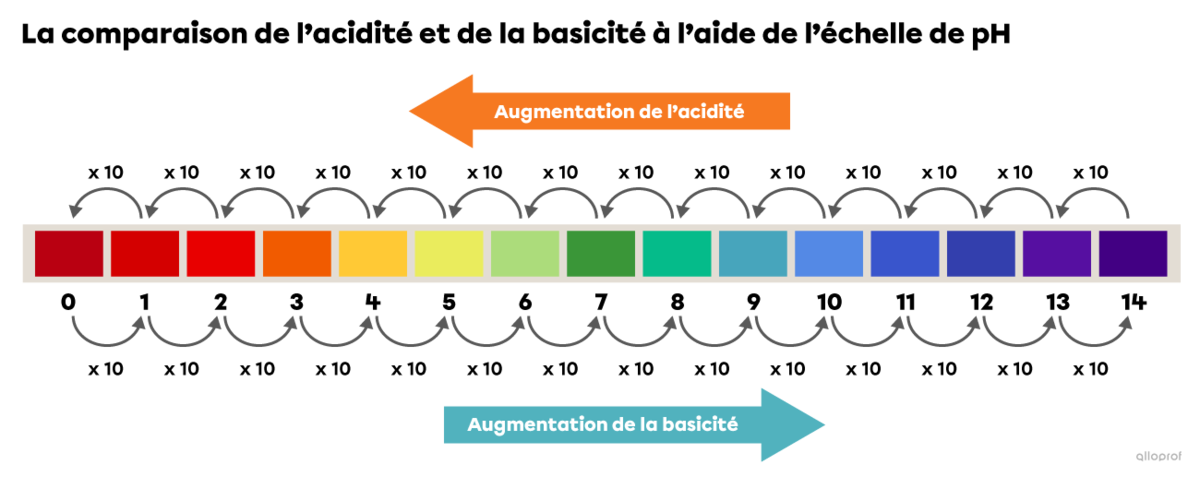
La variation d’une unité sur l’échelle de pH entraine la variation de l’acidité ou de la basicité d’une solution d’un facteur 10.
-
La diminution d’une unité sur l’échelle de pH signifie que l’acidité est multipliée par 10.
-
L’augmentation d’une unité sur l’échelle de pH signifie que la basicité est multipliée par 10.
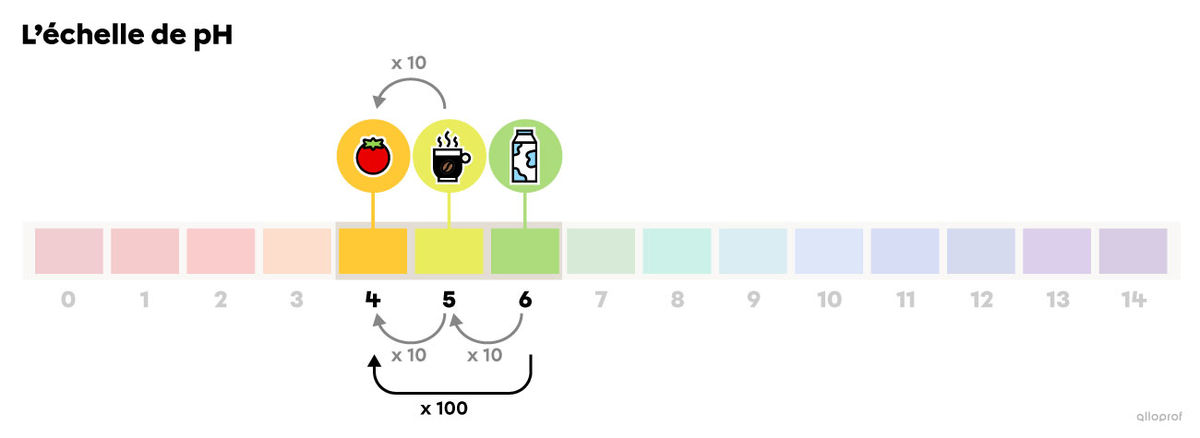
Le jus de tomates, dont le pH est 4, est 10 fois plus acide que le café, dont le pH est 5, puisque la variation est une diminution de 1 unité sur l’échelle de pH.
Le jus de tomates est 100 fois plus acide que le lait, dont le pH est 6, puisqu’il y a une diminution de 2 unités sur l’échelle de pH |(10\ \times 10=100).|
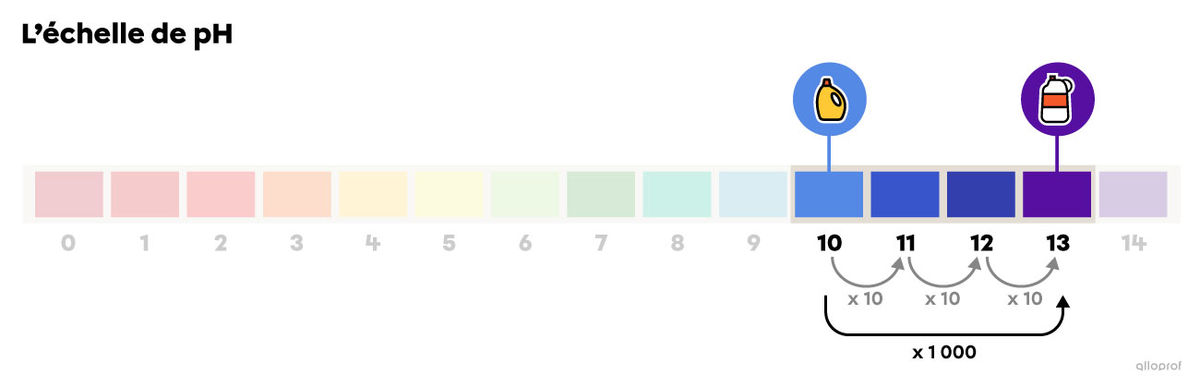
Afin de comparer un détergent à lessive (pH de 10) et l’eau de Javel (pH de 13), réponds aux questions suivantes.
-
Laquelle des deux substances est la plus basique?
-
Quelle est la variation de la basicité entre les deux substances?
-
Selon l’échelle de pH, plus le pH est grand, plus la substance est basique. L’eau de Javel est la substance la plus basique, car le pH de 13 est plus grand que le pH de 10.
-
Pour passer d’un pH de 10 à un pH de 13, on fait un bond de 3 unités sur l’échelle de pH. Puisque |(10\ \times 10\ \times10= 10^3 =1\ 000),| l’eau de Javel est 1 000 fois plus basique que le détergent à lessive. On peut aussi dire que le détergent à lessive est 1 000 fois moins basique que l’eau de Javel.
Il est possible de déterminer la concentration molaire des ions |\text{H}^+| d’une solution aqueuse à l’aide du pH de cette solution. Pour ce faire, on utilise la formule suivante.
|[\text{H}^+]=10^\text{-pH}|
où
|[\text{H}^+]\ :| concentration en ions |\text{H}^+| en moles par litre |(\text{mol/L})|
|\text{pH}\ :| valeur du pH
Une solution aqueuse d’acide chlorhydrique |(\text{HCl})| a un pH de |2{,}5.| Voici l’équation de dissociation de l’acide chlorhydrique dans l’eau.
||\text{HCl}_\text{(aq)}\rightarrow\text{H}^+_\text{(aq)}+\text{Cl}^-_\text{(aq)}||
Quelle est la concentration en ions |\text{H}^+| de cette solution?
On identifie les données.
|\begin{align} \text{pH} &=\ 2{,}5\\ [\text{H}^+] &=\ ?\ \text{mol/L}\end{align}|
On détermine la formule à utiliser.
|[\text{H}^+]=10^\text{-pH}|
On remplace la variable.
|[\text{H}^+]=10^{-2,5}|
On résout l’équation.
|[\text{H}^+]\approx0{,}003\,2\ \text{mol/L}|
La solution d’acide chlorhydrique a une concentration en ions |\text{H}^+| d’environ |0{,}003\,2\ \text{mol/L}.|
Lorsque la concentration en ions |\text{H}^+| d’une solution est exprimée en notation scientifique dont le premier facteur est 1, on peut déterminer le pH de cette solution en repérant l’exposant.
| |[\text{H}^+]| en |\text{mol/L}| | pH |
|---|---|
| |1\ \times\ 10^{-\color{#7CCA51}{1}}| | |\color{#7CCA51}1| |
| |1\ \times\ 10^{-\color{#7CCA51}{2}}| | |\color{#7CCA51}2| |
| |1\ \times\ 10^{-\color{#7CCA51}{3}}| | |\color{#7CCA51}3| |
| |1\ \times\ 10^{-\color{#7CCA51}{4}}| | |\color{#7CCA51}4| |
| |1\ \times\ 10^{-\color{#7CCA51}{5}}| | |\color{#7CCA51}5| |
| |1\ \times\ 10^{-\color{#7CCA51}{6}}| | |\color{#7CCA51}6| |
| |1\ \times\ 10^{-\color{#7CCA51}{7}}| | |\color{#7CCA51}7| |
| |1\ \times\ 10^{-\color{#7CCA51}{8}}| | |\color{#7CCA51}8| |
| |1\ \times\ 10^{-\color{#7CCA51}{9}}| | |\color{#7CCA51}9| |
| |1\ \times\ 10^{-\color{#7CCA51}{10}}| | |\color{#7CCA51}{10}| |
| |1\ \times\ 10^{-\color{#7CCA51}{11}}| | |\color{#7CCA51}{11}| |
| |1\ \times\ 10^{-\color{#7CCA51}{12}}| | |\color{#7CCA51}{12}| |
| |1\ \times\ 10^{-\color{#7CCA51}{13}}| | |\color{#7CCA51}{13}| |
| |1\ \times\ 10^{-\color{#7CCA51}{14}}| | |\color{#7CCA51}{14}| |
Cette astuce exprime le fait que le pH est une fonction logarithmique. Pour en savoir plus sur le calcul du pH, tu peux consulter la fiche suivante.
Un indicateur acidobasique est une substance qui a la propriété de changer de couleur en fonction du pH.
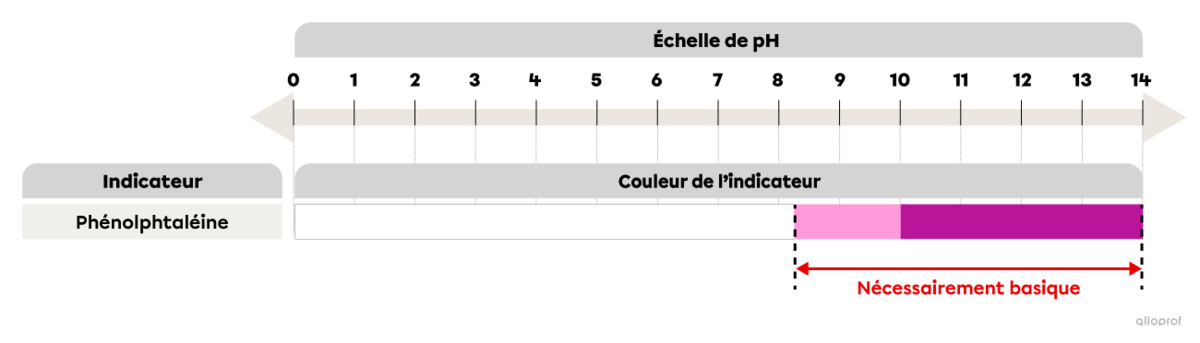
La phénolphtaléine est un indicateur qui peut être utilisé pour déterminer si une solution est basique. Il suffit d’en déposer quelques gouttes dans la solution en question et on observe s’il y a un changement de couleur.
-
Si la phénolphtaléine reste incolore, on ne peut pas déterminer si la solution est acide (pH inférieur à 7), neutre (pH égal à 7) ou basique (dans ce cas, pH entre 7 et 8,2).
-
Si l’indicateur devient rose, cela signifie que le pH de la solution se situe entre 8,2 et 10 et que la solution est basique.
-
Si l’indicateur devient fushia, cela signifie que le pH est supérieur à 10 et que la solution est basique.
En bref, si la phénolphtaléine devient rose ou fushia lorsqu’elle est mélangée à une solution, cette solution est nécessairement basique.
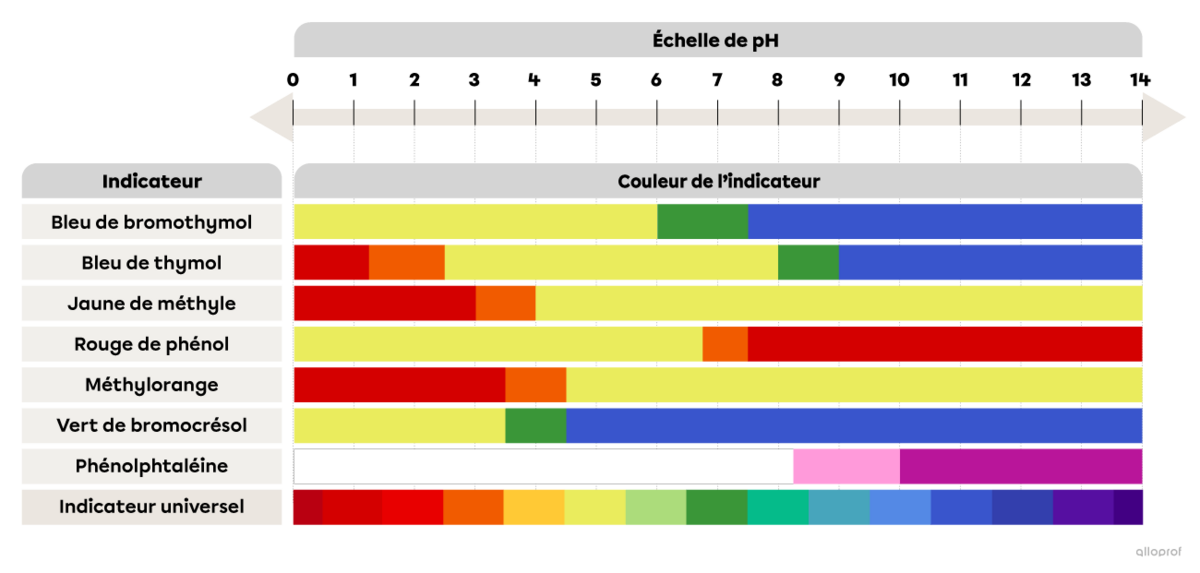
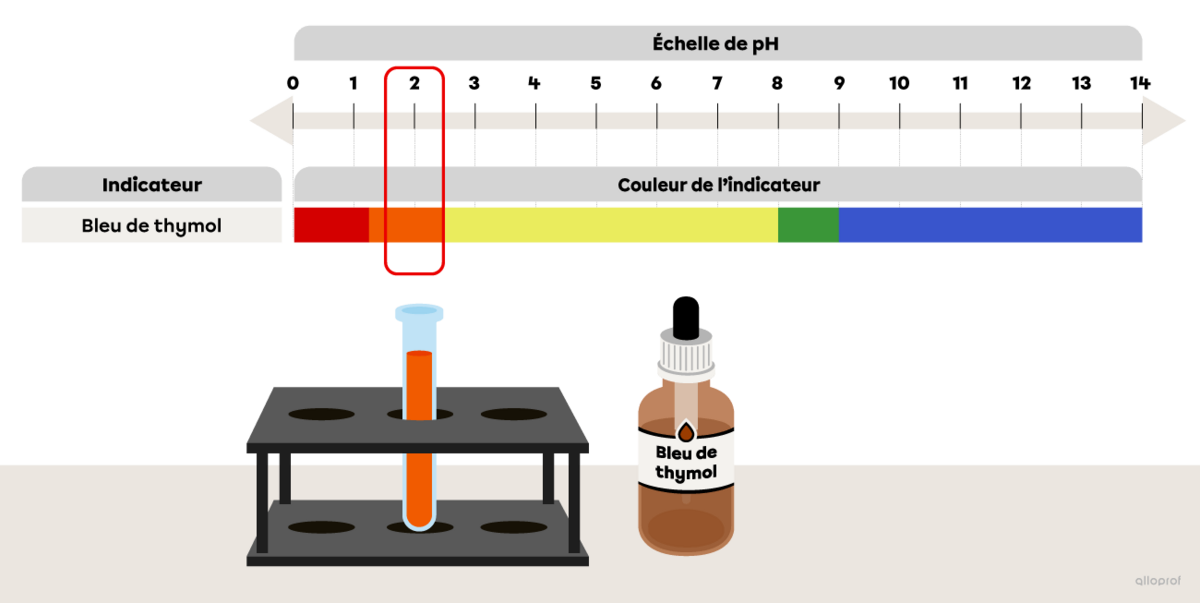
Dans une éprouvette remplie de jus de citron de pH 2, on ajoute quelques gouttes d’un indicateur acidobasique : le bleu de thymol. On s'assure que le bleu de thymol soit bien mélangé avec le jus de citron et on observe le changement de couleur.
En te référant à l’image La couleur de quelques indicateurs acidobasiques en fonction du pH, détermine quelle sera la couleur du bleu de thymol après avoir été mélangé avec le jus de citron.

Pour répondre à la question, on doit repérer la couleur du bleu de thymol lorsque le pH est de 2. Cette couleur correspond à celle de l’échantillon de jus de citron mélangé à l’indicateur. Ensuite, on répond à la question.
Dans le jus de citron, le bleu de thymol devient orange.
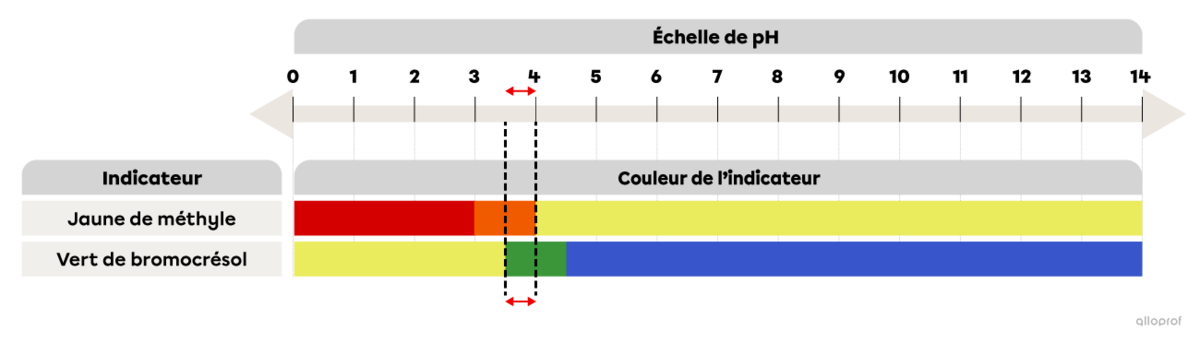
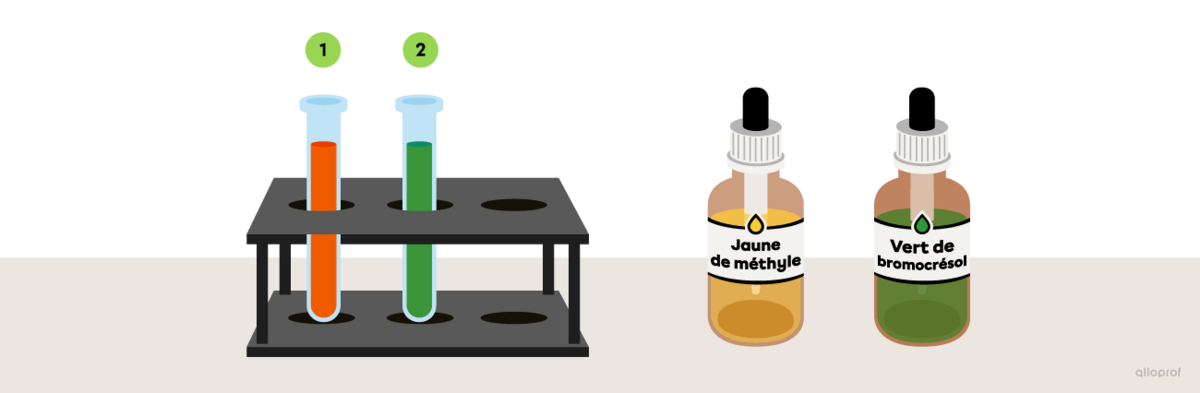
On ajoute quelques gouttes de jaune de méthyle à une substance inconnue et la solution devient orange. Dans une deuxième éprouvette, on ajoute du vert de bromocrésol et la solution inconnue devient verte.
En te référant à l’image La couleur de quelques indicateurs acidobasiques en fonction du pH, détermine dans quel intervalle se situe la valeur du pH de cette substance inconnue.
-
Puisque le jaune de méthyle devient orange lorsqu’il est mélangé à la substance inconnue, on peut dire que le pH de la substance se situe entre 3,0 et 4,0.
-
Puisque le vert de bromocrésol devient vert lorsqu’il est mélangé à la substance inconnue, on peut dire que le pH de la substance se situe entre 3,5 et 4,5.
En tenant compte de la réaction des deux indicateurs acidobasiques, on peut conclure que le pH de la substance inconnue se situe environ entre 3,5 et 4,0.