La stœchiométrie est l'étude des proportions selon lesquelles des substances interagissent dans une réaction chimique.
-
Les coefficients stœchiométriques sont des nombres placés devant les formules chimiques des substances dans une équation chimique. Ils indiquent les proportions selon lesquelles les substances interagissent dans une réaction chimique.
-
Les calculs stœchiométriques sont des calculs où on utilise la proportionnalité entre le rapport des coefficients stœchiométriques et celui des quantités (en moles ou en nombres de particules) pour calculer les quantités de réactifs et de produits impliquées dans une réaction chimique.
L'équation chimique balancée d'une réaction chimique permet de déterminer les proportions selon lesquelles les réactifs et les produits interagissent.
Dans une équation chimique balancée, le rapport entre les coefficients stœchiométriques de deux substances est proportionnel au rapport de leurs quantités respectives (en moles ou en nombres de particules) impliquées dans la réaction.
Dans la réaction suivante, le rapport entre les coefficients stœchiométriques des substances |\text{A}| et |\text{C}| est proportionnel au rapport des quantités exprimées en moles.
||\begin{align}\color{#3A9A38}{a}\text{A}\ +\ \color{#3A9A38}{b}{\text{B}}&\rightarrow \color{#3A9A38}{c}\text{C}\ +\ \color{#3A9A38}{d}\text{D}\\\\ \dfrac{\color{#3A9A38}{a}}{\color{#3A9A38}{c}}&=\dfrac {\color{#FA7921}{n_{\text{A}}}}{\color{#FA7921}{n_{C}}}\end{align}||
où
|\color{#FA7921}{n}:| quantité en moles (mol)
|\text{A, B, C, D}:| formules chimiques des réactifs et des produits
|\color{#3A9A38}{a, b, c,d}:| coefficients stœchiométriques
Le rapport entre les coefficients stœchiométriques est proportionnel au rapport des quantités, seulement lorsque les quantités sont exprimées en nombre de moles ou en nombre de particules.

Le rapport entre les coefficients stœchiométriques n’est pas proportionnel au rapport entre les masses.
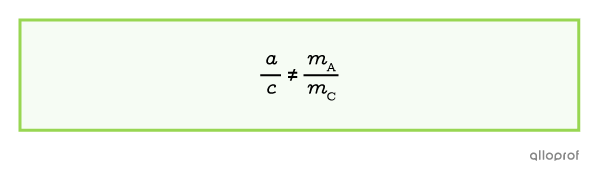
Le rapport entre deux coefficients stœchiométriques est également appelé rapport molaire ou rapport stœchiométrique.
Selon l’équation chimique balancée suivante, combien de moles de diazote |(\text{N}_2)| sont produites lors de la décomposition de |2{,}25\ \text{mol}| d’ammoniac |(\text{NH}_3)|?
||\color{#3A9A38}{2}\ \text{NH}_3\rightarrow\text{N}_2\ +\ \color{#3A9A38}{3}\ \text{H}_2||
-
On identifie les données.
||\begin{align}n_{\text{NH}_3}&=2{,}25\ \text{mol}\\
n_{\text{N}_2}&=\ ?\ \text{mol}\end{align}|| -
On détermine la proportion entre le rapport des coefficients stœchiométriques et le rapport des quantités.
Dans la réaction chimique précédente, le coefficient stœchiométrique de l’ammoniac |(\text{NH}_3)| est de |\color{#3A9A38}{2}| et celui du diazote |(\text{N}_2)| est de |\color{#3A9A38}{1}.| Les coefficients stœchiométriques indiquent que |\text{NH}_3| et |\text{N}_2| interagissent dans un rapport de 2 pour 1. Ce rapport est proportionnel et donc égal au rapport des quantités respectives exprimées en nombre de moles |(n).|
||\frac{\color{#3A9A38}{2}}{\color{#3A9A38}{1}}= \frac{n_{\text{NH}_3}}{n_{\text{N}_2}}|| -
On remplace la variable connue.
||\frac{\color{#3A9A38}{2}}{\color{#3A9A38}{1}}= \frac{2{,}25\ \text{mol}}{n_{\text{N}_2}}|| -
On résout l’équation.
||\begin{align}n_{\text{N}_2}&=\dfrac{\color{#3A9A38}{1}\times2{,}25}{\color{#3A9A38}{2}}\\ n_{\text{N}_2}&=1{,}13\ \text{mol}\end{align}||
Une quantité de |1{,}13\ \text{mol}| de |\text{N}_2| a été produite lors de la décomposition de |2{,}25\ \text{mol}| de |\text{NH}_3.|
Pour faciliter la résolution d’un problème de stœchiométrie, on peut utiliser un tableau pour organiser les informations connues, les informations recherchées et les valeurs calculées. Cette méthode de travail, parfois appelée la méthode du tableau, permet de bien visualiser les calculs stœchiométriques et de ne pas oublier de faire les conversions d’unités lorsque nécessaire.
Ce tableau comprend généralement cinq lignes où l'on présente :
-
l’équation chimique balancée,
-
les coefficients stœchiométriques,
-
les nombres de moles |(n),|
-
les masses molaires |(M)| et
-
les masses |(m).|

Une fois le tableau construit, il est recommandé de résoudre le problème en suivant les étapes suivantes.
-
Inscrire l’équation chimique balancée de la réaction et ajouter les coefficients dans le tableau.
-
Ajouter les informations fournies dans l’énoncé du problème.
-
Calculer et inscrire la masse molaire de chaque substance concernée par le problème.
-
Convertir les masses connues de réactif ou de produit en moles.
-
Identifier dans le tableau les valeurs à calculer pour résoudre le problème.
-
Calculer le nombre de moles d’un réactif ou d’un produit désiré à l’aide d’un calcul stœchiométrique.
-
Convertir le nombre de moles en grammes.
Selon le problème à résoudre, les étapes 3, 4 et 7 peuvent être non nécessaires.
L’électrolyse d’une solution d’alumine permet de produire de l’aluminium selon la réaction suivante.
||\text{Al}_2\text{O}_{3_{(aq)}}+\text{C}_{_{(s)}}\rightarrow\text{Al}_{_{(l)}}+\text{CO}_{2_{(g)}}||
Quelle masse de carbone |(\text{C})| permet de produire |100\ \text{g}| d'aluminium |(\text{Al})|?
-
Inscrire l’équation chimique balancée de la réaction et ajouter les coefficients dans le tableau.

-
Ajouter les informations connues et fournies dans l’énoncé du problème.
Dans ce problème, on sait qu’une masse de |100\ \text{g}| d'aluminium |(\text{Al})| est produite.

-
Calculer et inscrire les masses molaires des différentes substances concernées par le problème.
Dans ce problème, on s’intéresse au carbone |(\text{C})| et à l’aluminium |(\text{Al}).| On inscrit la masse molaire de chacun.

Attention : Le calcul de la masse molaire ne doit pas tenir compte des coefficients stœchiométriques. -
Convertir les masses connues de réactif ou de produit en moles.
On calcule le nombre de moles d’aluminium |(n_\text{Al})| qui correspond à une masse |(m_\text{Al})| de |100\ \text{g}| à l’aide de la masse molaire |(M_\text{Al}).|
||\begin{align}M_{\text{Al}}=\dfrac{m_\text{Al}}{n_{\text{Al}}}\ \Rightarrow\ n_\text{Al}&=\dfrac{m_\text{Al}}{M_\text{Al}}\\\\
n_\text{Al}&=\dfrac{100\ \text{g}}{26{,}98\ \text{g/mol}}\\\\
n_\text{Al}&=3{,}71\ \text{mol}\end{align}||

-
Identifier dans le tableau les valeurs à calculer pour résoudre le problème.
Pour résoudre le problème, on doit calculer le nombre de moles de carbone et sa masse.

-
Calculer le nombre de moles d’un réactif ou d’un produit désiré à l’aide d’un calcul stœchiométrique.
On utilise la proportion entre le rapport des coefficients stœchiométriques et celui des quantités exprimées en moles pour calculer le nombre de moles de carbone |(\text{C}),| lorsque |3{,}71\ \text{mol}| d’aluminium |(\text{Al})| sont produites.

||\begin{align}\dfrac{3}{4}&=\dfrac{n_{\text{C}}}{3{,}71\ \text{mol}}\\\\
n_{\text{C}}&=\dfrac{3\times3{,}71\ \text{mol}}{4}\\\\
n_{\text{C}}&=2{,}78\ \text{mol}\end{align}||
-
Convertir le nombre de moles en grammes.
On calcule la masse de |2{,}78\ \text{mol}| de carbone |(\text{C})| à l’aide de sa masse molaire.
||\begin{align}
M_{\text{C}}=\dfrac{m_\text{C}}{n_{\text{C}}}\ \Rightarrow\
m_{\text{C}}&={n_{\text{C}}}\times{M_\text{C}}\\m_{\text{C}}&={2{,}78\ \text{mol}}\times{12{,}01\ \text{g/mol}}\\m_{\text{C}}&=33{,}39\ \text{g}\end{align}||

Une masse de |33{,}39\ \text{g}| de carbone permet de produire |100\ \text{g}| d'aluminium.
Pour valider ta compréhension à propos de la résolution d'un problème de stœchiométrie de façon interactive, consulte la MiniRécup suivante.
