La périodicité des propriétés des éléments dans le tableau périodique correspond à la façon dont les propriétés physiques et chimiques des éléments se répètent régulièrement d'une période à l'autre.
Les propriétés chimiques ne sont pas constantes à l’intérieur d'une même période.
La masse atomique représente la masse de toutes les particules formant l'atome, soit les protons, les électrons et les neutrons.
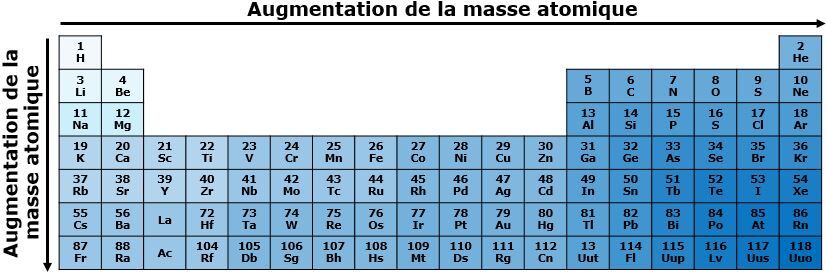
Dans une même période, la masse atomique augmente de gauche à droite dans le tableau périodique. Puisque le nombre de particules de l'atome augmente de gauche à droite avec le numéro atomique, la masse atomique augmente également dans la même direction, car un plus grand nombre de particules implique nécessairement une plus grande masse.
Dans une même famille, la masse atomique augmente de haut en bas dans le tableau périodique. Comme le numéro atomique augmente de haut en bas, un plus grand nombre de protons se retrouvent dans les atomes situés dans le bas du tableau périodique, ce qui implique nécessairement une plus grande masse atomique.
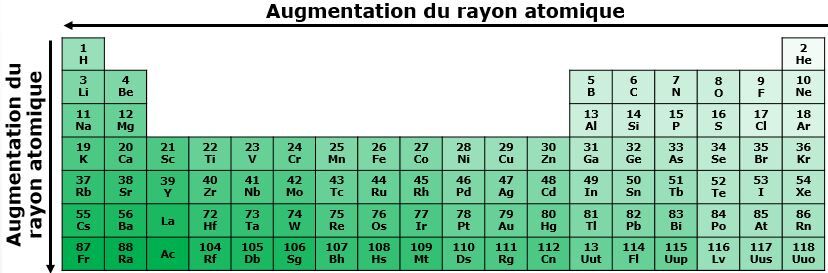
Le rayon atomique représente le rayon de l’atome ou, en d'autres mots, le rayon de la sphère que forme l’atome.
Plus le rayon atomique est grand, plus le volume de l'atome est grand.
Dans une même période, le rayon atomique augmente de droite à gauche dans le tableau périodique. Lorsqu'on se déplace vers la droite, le numéro atomique augmente, ce qui signifie qu'un plus grand nombre de protons est présent dans le noyau. Ces charges positives exercent une force d'attraction plus grande sur les électrons situés sur les couches électroniques, ce qui les rapproche du noyau. Le rayon atomique est donc plus petit pour ces éléments.
Dans une même famille, le rayon atomique augmente de haut en bas dans le tableau périodique. En se déplaçant vers le bas du tableau périodique, le nombre de couches électroniques augmentent. Les électrons se retrouvent donc de plus en plus loin du noyau, ce qui contribue à l'augmentation du rayon atomique.
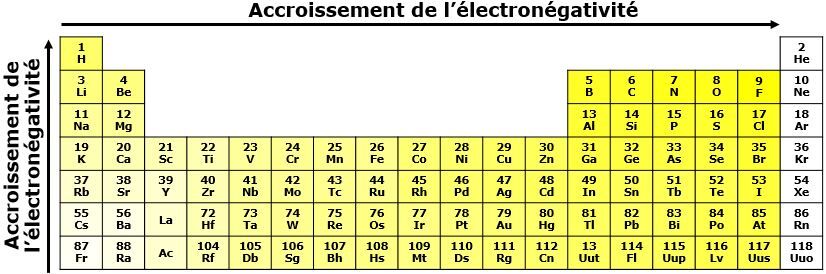
L'électronégativité est la force avec laquelle le noyau d’un atome attire les électrons impliqués dans une liaison chimique.
Plus l'électronégativité est grande, plus il est facile pour l’atome de s’approprier des électrons des atomes voisins.
Dans une même période, l'électronégativité augmente de gauche à droite dans le tableau périodique. Au fur et à mesure que l'on se déplace vers la droite, les atomes ont tendance à gagner des électrons afin d'acquérir une configuration électronique stable. Ainsi, les non-métaux ont une plus forte tendance à acquérir des électrons, alors que cette tendance est plus faible pour les éléments à gauche.
Dans une même famille, l'électronégativité augmente du bas vers le haut du tableau périodique. Puisque les atomes du bas du tableau périodique sont plus gros, la force d'attraction exercée par le noyau est plus faible étant donné la plus grande distance entre les charges positives du noyau et les électrons situés sur la dernière couche électronique. Par conséquent, plus l'atome est grand, plus l'électronégativité diminue.
Les gaz inertes n'ont aucune électronégativité, car ces atomes ne cherchent pas à attirer des électrons étant donné leur dernière couche électronique saturée. Puisque ces atomes respectent déjà la règle de l'octet, ils ne chercheront pas à attirer des nouveaux électrons.
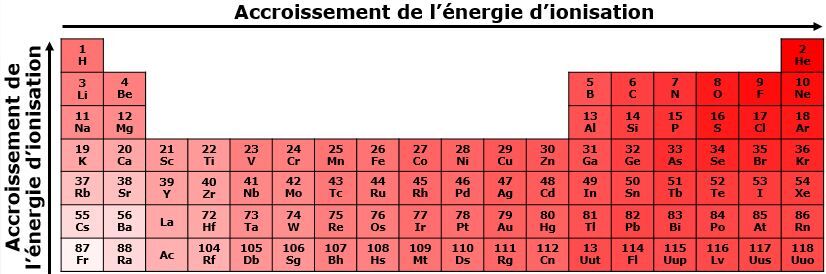
L'énergie d'ionisation représente l’énergie nécessaire pour arracher un électron à un atome.
Plus elle est grande, plus il est difficile d’arracher un électron à cet atome.
De manière générale, dans une même période, l'énergie d'ionisation augmente de gauche à droite dans le tableau périodique. Dans les atomes situés à droite, le noyau atomique exerce une plus grande force sur les électrons. Ces électrons nécessitent donc une plus grande quantité d'énergie pour qu'ils soient arrachés. À l'opposé, les atomes situés à gauche dans le tableau périodique exercent une force plus faible sur les électrons, car les électrons sont plus loin du noyau et qu'un plus petit nombre de protons est présent dans le noyau.
De manière générale, dans une même famille, l'énergie d'ionisation augmente du bas vers le haut du tableau périodique. La quantité d'énergie nécessaire pour retirer un électron est plus petite pour les éléments du bas du tableau, car la force d'attraction entre les électrons de valence et le noyau est plus petite. Ces électrons étant moins attirés, il est plus facile de les arracher que dans un élément situé dans le haut du tableau.
Pour valider ta compréhension à propos du tableau périodique de façon interactive, consulte la MiniRécup suivante :
