Les règles d’écriture correspondent à un ensemble de règles qui permettent de déterminer la formule chimique d’un composé.
Les sections suivantes abordent les règles d’écriture des composés binaires qui comprennent un métal et un non-métal. Le fait de lier chimiquement un métal et un non-métal engendre des ions, c’est pourquoi on parle plus précisément de composés ioniques binaires.
Pour déterminer la formule chimique d’un composé ionique binaire à partir des éléments qui le composent, il faut avant tout déterminer la charge des ions qui constituent ce composé.
Afin de déterminer la charge d’un ion, on peut se fier à la règle de l’octet. Elle indique la tendance d’un élément à donner ou à accepter des électrons pour engendrer un ion.
Le tableau périodique suivant présente la ou les charges qu’un élément peut adopter lorsqu’il se trouve dans un composé ionique binaire. Le tableau concerne les éléments 1 à 54.
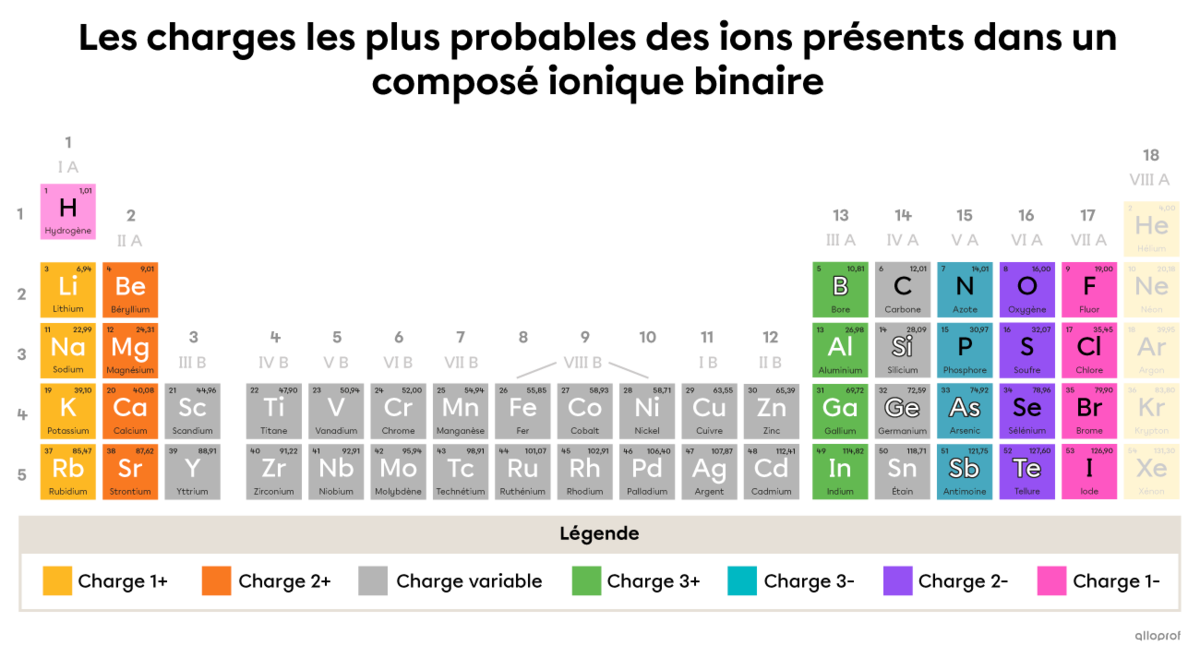
Les charges présentées dans ce tableau sont les charges les plus probables que peut adopter un ion dans un composé ionique binaire. D’autres charges sont possibles, bien qu’elles soient plus rares.
De plus, les charges présentes dans ce tableau s’appliquent aux composés ioniques binaires. Si un composé est non ionique, il n’y a pas d’ions formés. Si un composé est ionique, mais non binaire, les charges des ions qui le composent peuvent être différentes.
Dans un composé ionique binaire, quelle est la charge la plus probable d’un ion de magnésium?
Le magnésium |(\text{Mg})| est l’élément numéro 12 et fait partie de la famille II A. Il a donc 2 électrons de valence. Afin d’atteindre l’octet, il a tendance à donner ces 2 électrons, ce qui lui procure une charge de |2+| lorsqu’il se trouve sous forme d’ion. L’ion correspondant est |\text{Mg}^{2+}.|
Le tableau périodique précédent permet également de connaitre rapidement la charge la plus probable d’un ion de magnésium.

Dans un composé ionique binaire, quelle est la charge la plus probable d’un ion d’aluminium?
L’aluminium |(\text{Al})| est l’élément numéro 13 et fait partie de la famille III A. Il a donc 3 électrons de valence. Afin d’atteindre l’octet, il a tendance à donner ces 3 électrons, ce qui lui procure une charge de |3+| lorsqu’il se trouve sous forme d’ion. L’ion correspondant est |\text{Al}^{3+}.|
Le tableau périodique précédent permet également de connaitre rapidement la charge la plus probable d’un ion d’aluminium.

Dans un composé ionique binaire, quelle est la charge la plus probable d’un ion de cuivre?
Le cuivre |(\text{Cu})| est l’élément numéro 29. Grâce au tableau périodique précédent, on sait que, lorsque cet élément se trouve sous forme d’ion, différentes charges sont possibles. Il n’y a pas assez d’informations dans l’énoncé pour répondre à la question posée.
De plus, la règle de l’octet ne s’applique pas pour les métaux de transition (soit les métaux des familles 3 à 12), donc on ne peut pas déterminer la charge d’un ion de cuivre à partir de cette règle.

Afin de déterminer la formule chimique d’un composé ionique binaire à partir des éléments qui le composent, on peut suivre les règles d’écriture suivantes.
-
Déterminer la charge des ions correspondant aux éléments qui constituent le composé.
-
Déterminer le nombre de chaque ion nécessaire pour former un composé électriquement neutre. La somme des charges de tous les ions doit être égale à 0.
-
Écrire la formule chimique correspondante en écrivant le métal en premier et le non-métal en dernier.
Un composé comprend du calcium |(\text{Ca})| et du chlore |(\text{Cl}).| Quelle est la formule chimique de ce composé?
-
Dans ce composé ionique binaire, le calcium se trouve sous la forme d’un ion |\text{Ca}^{2+}| et le chlore se trouve sous la forme d’un ion |\text{Cl}^{-}.| On peut déterminer ceci grâce à la règle de l’octet et en se référant au tableau périodique.

-
Pour former un composé électriquement neutre, il faut que la somme des charges de tous les ions donne 0. Ainsi, si le composé comprend 1 ion |\text{Ca}^{2+}| et 2 ions |\text{Cl}^{-},| la somme des charges est nulle.

-
Le calcium |(\text{Ca})| est un métal, donc son symbole s’écrit en premier dans la formule chimique du composé. Le chlore |(\text{Cl})| est un non-métal, donc son symbole s’écrit en dernier dans la formule. Il y a 2 atomes de chlore |(\text{Cl}),| donc on indique un |2| en indice dans la formule.
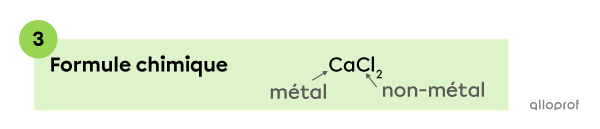
La formule chimique d’un composé comprenant du calcium |(\text{Ca})| et du chlore |(\text{Cl})| est donc |\text{CaCl}_{2}.|
Remarque : La charge des ions du composé |\text{CaCl}_2| n’est pas indiquée dans la formule. Ainsi, on n’écrit pas |\text{Ca}^{2+} \text{Cl}^{-}_2,| mais bien |\text{CaCl}_{2}.|
Un composé comprend du lithium |(\text{Li})| et de l’hydrogène |(\text{H}).| Quelle est la formule chimique de ce composé?
-
Dans ce composé ionique binaire, le lithium se trouve sous la forme d’un ion |\text{Li}^+| et l’hydrogène se trouve sous la forme d’un ion |\text{H}^{-}.| On peut déterminer ceci grâce à la règle de l’octet et en se référant au tableau périodique.

-
Pour engendrer un composé électriquement neutre, il faut que la somme des charges de tous les ions donne 0. Ainsi, si le composé comprend 1 ion |\text{Li}^+| et 1 ion |\text{H}^{-},| la somme des charges est nulle.

-
Le lithium |(\text{Li})| est un métal, donc son symbole s’écrit en premier dans la formule chimique. L’hydrogène |(\text{H})| est un non-métal, donc son symbole s’écrit en dernier dans la formule.
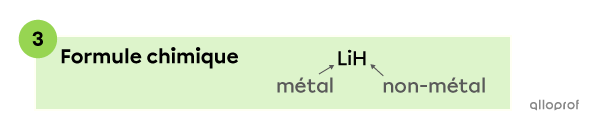
La formule chimique d’un composé comprenant du lithium |(\text{Li})| et de l’hydrogène |(\text{H})| est donc |\text{LiH}.|
Remarque : La charge des ions du composé |\text{LiH}| n’est pas indiquée dans la formule. Ainsi, on n’écrit pas |\text{Li}^{+} \text{H}^{-},| mais bien |\text{LiH}.|
Un composé comprend de l’aluminium |(\text{Al})| et de l’oxygène |(\text{O}).| Quelle est la formule chimique de ce composé?
-
Dans ce composé ionique binaire, l’aluminium se trouve sous la forme d’un ion |\text{Al}^{3+}| et l’oxygène se trouve sous la forme d’un ion |\text{O}^{2-}.| On peut déterminer ceci grâce à la règle de l’octet et en se référant au tableau périodique.

-
Pour engendrer un composé électriquement neutre, il faut que la somme des charges de tous les ions donne 0. Ainsi, si le composé comprend 2 ions |\text{Al}^{3+}| et 3 ions |\text{O}^{2-},| la somme des charges est nulle.

-
L’aluminium |(\text{Al})| est un métal, donc son symbole s’écrit en premier dans la formule chimique. L’oxygène |(\text{O})| est un non-métal, donc son symbole s’écrit en dernier dans la formule. Il y a 2 atomes d’aluminium |(\text{Al})| et 3 atomes d’oxygène |(\text{O})|, donc on indique un |2| et un |3| en indice dans la formule devant leurs atomes respectifs.
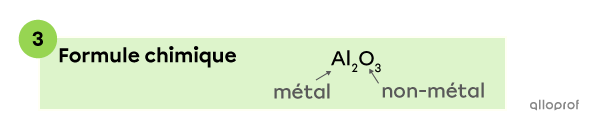
La formule chimique d’un composé comprenant de l’aluminium |(\text{Al})| et de l’oxygène |(\text{O})| est donc |\text{Al}_2 \text{O}_{3}.|
Remarque : La charge des ions du composé |\text{Al}_2 \text{O}_3| n’est pas indiquée dans la formule. Ainsi, on n’écrit pas |{\text{Al}^{3+}}_2 {\text{O}^{2-}}_{3},| mais bien |\text{Al}_2 \text{O}_{3}.|