Les lois simples des gaz décrivent les propriétés physiques des gaz telles que la pression |(P),| le volume |(V),| le nombre de moles |(n)| et la température |(T).|
Il y a 5 lois simples. Chacune d’elles décrit la relation entre deux propriétés alors que les autres sont constantes.
Le tableau suivant résume les lois simples. Pour voir tous les détails d’une loi, clique sur son nom.
|
Nom |
Description et graphique | Formules |
|---|---|---|
|
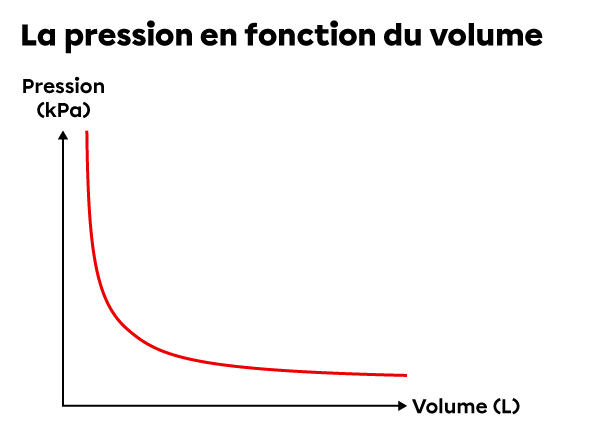
La pression |(P)| est inversement proportionnelle au volume |(V)| si le nombre de moles |(n)| et la température |(T)| sont constants. |
Si |n| et |T| ne varient pas : ||\begin{align} |
|
|
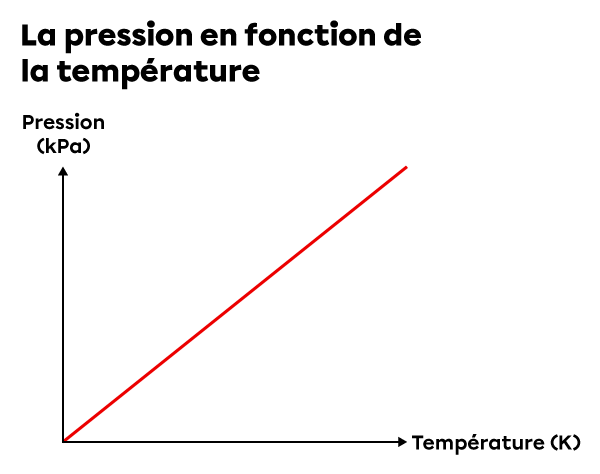
La pression |(P)| est proportionnelle à la température absolue |(T)| si le nombre de moles |(n)| et le volume |(V)| sont constants. |
Si |n| et |V| ne varient pas : ||\begin{align} |
|
|
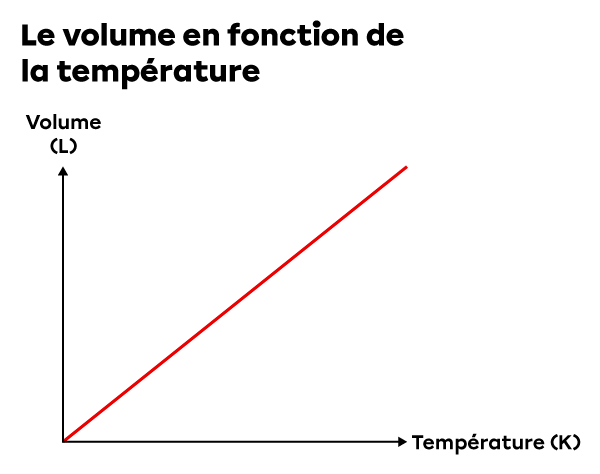
Le volume |(V)| est proportionnel à la température absolue |(T)| si le nombre de moles |(n)| et la pression |(P)| sont constants. |
Si |n| et |P| ne varient pas : ||\begin{align} |
|
|
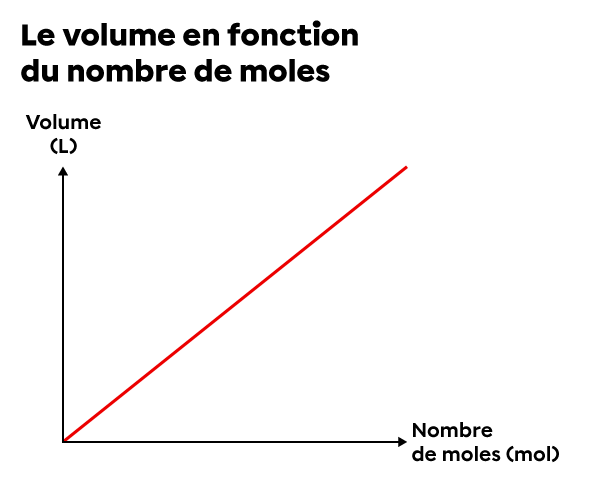
Le volume |(V)| est proportionnel au nombre de moles |(n)| si la pression |(P)| et la température |(T)| sont constantes. |
Si |P| et |T| ne varient pas : ||\begin{align} |
|
|
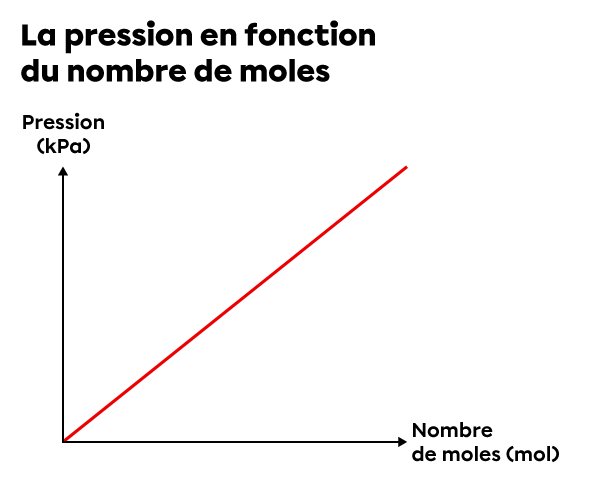
La pression |(P)| est proportionnelle au nombre de moles |(n)| si le volume |(V)| et la température |(T)| sont constants. |
Si |V| et |T| ne varient pas : ||\begin{align} |
Lorsque les lois simples sont mises en commun, on obtient la loi générale des gaz |\left(\dfrac{P_1V_1}{n_1T_1}=\dfrac{P_2V_2}{n_2T_2}\right)| et la loi des gaz parfaits |(PV=nRT).|
Les lois simples des gaz s’appliquent uniquement pour les gaz parfaits.
Autrement dit, les valeurs calculées à l’aide des lois simples correspondent approximativement aux valeurs réelles, tant que la température du gaz n’est pas trop basse et que sa pression n’est pas trop élevée.